GENOTONORM KABIPEN 12 mg PÓ E SOLVENTE PARA SOLUÇÃO INJETÁVEL

Como utilizar GENOTONORM KABIPEN 12 mg PÓ E SOLVENTE PARA SOLUÇÃO INJETÁVEL
Traduzido com IA
Esta informação é fornecida apenas para fins informativos e não substitui a consulta de um médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
Mostrar originalConteúdo do folheto informativo
Introdução
Prospecto: informação para o utilizador
GENOTONORM KABIPEN 5,3 mg e 12 mg pó e dissolvente para solução injetável
somatropina
Leia todo o prospecto atentamente antes de começar a usar este medicamento, porque contém informações importantes para si.
- Conserva este prospecto, porque pode ter que voltar a lê-lo.
- Se tiver alguma dúvida, consulte o seu médico ou farmacêutico.
- Este medicamento foi-lhe prescrito apenas para si, e não deve dá-lo a outras pessoas, mesmo que tenham os mesmos sintomas que si, porque pode prejudicá-las.
- Se considera que algum dos efeitos adversos que sofre é grave ou se apercebe de qualquer efeito adverso não mencionado neste prospecto, informe o seu médico ou farmacêutico.
Conteúdo do prospecto:
- O que é Genotonorm Kabipen e para que é utilizado
- O que precisa saber antes de começar a usar Genotonorm Kabipen
- Como usar Genotonorm Kabipen
- Posíveis efeitos adversos
- Conservação de Genotonorm Kabipen
- Conteúdo do envase e informações adicionais
1. O que é Genotonorm Kabipen e para que é utilizado
Genotonorm Kabipen é uma hormona recombinante de crescimento humano (também conhecida como somatropina). Tem a mesma estrutura que a hormona de crescimento humana, a qual é necessária para o crescimento dos ossos e dos músculos. Também ajuda a que o tecido gordo e muscular se desenvolva nas quantidades adequadas. O facto de ser recombinante significa que não procede nem de tecido humano nem animal.
Em crianças, Genotonorm Kabipen é utilizado para o tratamento de distúrbios do crescimento:
- Se não cresce de forma adequada ou se não possui suficiente hormona de crescimento própria.
- Em caso de síndrome de Turner. O síndrome de Turner é uma alteração cromossómica que se dá nas raparigas e pode afetar o crescimento – o seu médico indicar-lhe-á se o padece.
- Em caso de insuficiência renal crónica. Se o rim perde a sua capacidade para funcionar adequadamente, o crescimento pode ver-se afetado.
- Em caso de síndrome de Prader-Willi (uma alteração cromossómica). A hormona de crescimento ajudá-lo-á a crescer se ainda se encontra em período de crescimento e também melhorará a composição corporal. O excesso de gordura diminuirá e a perda de massa muscular melhorará.
- Em caso de ter nascido pequeno ou com pouco peso. A hormona de crescimento pode ajudá-lo a crescer se ainda não foi capaz de atingir ou manter o crescimento normal à idade de 4 anos ou posterior.
Em adultos, Genotonorm Kabipen é utilizado para o tratamento de pessoas com uma marcada deficiência de hormona de crescimento. Isto pode iniciar-se na idade adulta, ou pode ter-se iniciado na infância e continuar até à idade adulta.
Se esteve em tratamento com Genotonorm Kabipen por uma deficiência de hormona de crescimento durante a infância, deve reavaliar a hormona de crescimento após completar a fase de crescimento. Se for confirmada a deficiência severa de hormona de crescimento, o seu médico propor-lhe-á a continuação do tratamento com Genotonorm Kabipen.
Este medicamento só pode ser prescrito por um médico com experiência no tratamento com hormona de crescimento e que lhe tenha confirmado o diagnóstico.
2. O que precisa saber antes de começar a usar Genotonorm Kabipen
Não use Genotonorm Kabipen e contacte o seu médico se
- É alérgico (hipersensível) à somatropina ou a algum dos outros componentes de Genotonorm Kabipen.
- Padece um tumor ativo (cancro). Os tumores devem estar inativos e deve ter finalizado o tratamento antitumoral antes de começar o tratamento com Genotonorm.
- Está gravemente doente (por exemplo, complicações após uma cirurgia a coração aberto, cirurgia abdominal, insuficiência respiratória aguda, traumatismo acidental ou alguma situação similar). Se está a ponto de se submeter ou se submeteu a uma operação importante ou vai ingressar no hospital por qualquer razão, diga-o ao seu médico e recorde ao resto dos médicos que o examinem que utiliza hormona de crescimento.
- Já finalizou o seu período de crescimento (epífises fechadas) e lhe foi prescrito Genotonorm Kabipen para estimular o crescimento.
Tenha especial cuidado com Genotonorm Kabipen e contacte o seu médico
- Se tem risco de desenvolver diabetes, o seu médico vigiará os níveis de açúcar no sangue durante o tratamento com Genotonorm Kabipen.
- Se tem diabetes, deve vigiar cuidadosamente os níveis de açúcar no sangue durante o tratamento com Genotonorm Kabipen e ver os resultados com o seu médico para determinar se precisa mudar a dosagem dos medicamentos para a diabetes.
- Após o início do tratamento com Genotonorm Kabipen, alguns pacientes podem precisar começar tratamento com hormona tiroideia.
- Se está a receber tratamento com hormonas tiroideias, pode ser necessário ajustar a dosagem da hormona tiroideia.
- Se está em tratamento com hormona de crescimento para estimular o crescimento e coxeia, ou se começa a coxear porque tem dor na anca durante o tratamento com hormona de crescimento, deve informar o seu médico.
- Se se produz um aumento da pressão intracraniana (com sintomas tais como fortes dores de cabeça, problemas de visão ou vómitos) deve informar o seu médico sobre isso.
- Se o seu médico confirmar que desenvolveu inflamação dos músculos perto da área de injeção devido ao conservante metacresol, deve utilizar outra apresentação de Genotonorm que não contenha metacresol.
- Se está a receber Genotonorm Kabipen por uma deficiência de hormona de crescimento após um tumor prévio (canço), deve ser submetido a uma revisão periódica por possíveis recorrências do tumor ou qualquer outro cancro.
- Se sofre dor abdominal que se torna mais intensa, deve informar o seu médico.
- A experiência em pacientes com mais de 80 anos de idade é limitada. As pessoas de idade avançada podem ser mais sensíveis à ação de Genotonorm Kabipen, e por tanto, podem ter mais predisposição para desenvolver efeitos adversos.
Crianças com insuficiência renal crónica:
- O seu médico examinará a função renal e a velocidade de crescimento antes de iniciar o tratamento com Genotonorm Kabipen. O tratamento médico para a doença renal deve continuar. O tratamento com Genotonorm Kabipen deve ser suspenso em caso de transplante de rim.
Crianças com síndrome de Prader-Willi:
- O seu médico dar-lhe-á restrições na dieta para controlar o peso.
- O seu médico realizará uma exploração antes de começar o tratamento com Genotonorm Kabipen para determinar se padece obstrução das vias respiratórias altas, apneia do sono (quando a respiração se interrompe durante o sono) ou infecções respiratórias.
- Se durante o tratamento apresenta sinais de obstrução das vias respiratórias altas (incluindo o início ou aumento de roncos), o seu médico necessitará examiná-lo e poderá interromper o tratamento com Genotonorm Kabipen.
- Durante o tratamento, o seu médico vigiará qualquer sinal de escoliose, um tipo de deformação da coluna.
- Se durante o tratamento desenvolve uma infecção pulmonar, diga-o ao seu médico para que possa tratar a infecção.
Crianças nascidas pequenas ou com peso baixo:
- Se nasceu pequeno ou com peso baixo e tem entre 9 e 12 anos, consulte especificamente o seu médico sobre a puberdade e o tratamento com este produto.
- O seu médico realizará análises de açúcar e de insulina no sangue antes de começar o tratamento e uma vez por ano enquanto este durar.
- O tratamento deve continuar até que finalize a fase de crescimento.
Uso em desportistas
Este medicamento contém somatropina que pode produzir um resultado positivo nos testes de controlo de dopagem.
Uso de outros medicamentos
Informa o seu médico ou farmacêutico se está a utilizar ou utilizou recentemente qualquer outro medicamento, mesmo os adquiridos sem receita.
Advertências e precauções
Consulte o seu médico ou farmacêutico antes de começar a usar Genotonorm.
Se está a receber tratamento de substituição com glucocorticoides, deve consultar o seu médico regularmente, pois pode ser necessário um ajuste da dosagem de glucocorticoide.
Informa o seu médico se está a utilizar:
- medicamentos para o tratamento da diabetes
- hormonas tiroideias
- hormonas sintéticas adrenais (corticosteroides)
- estrógenos administrados por via oral ou outras hormonas sexuais
- ciclosporina (medicamento que debilita o sistema imunológico após um transplante)
- medicamentos para o controlo da epilepsia (anticonvulsivantes)
O seu médico pode precisar realizar um ajuste da dosagem destes medicamentos ou da dosagem de Genotonorm Kabipen.
Gravidez e lactação
Não utilize Genotonorm Kabipen se está grávida, acredita que possa estar grávida ou está a tentar engravidar.
Consulte o seu médico antes de utilizar este medicamento enquanto está em período de amamentação.
Consulte o seu médico ou farmacêutico antes de utilizar qualquer medicamento.
Genotonorm Kabipen contém sódio
Este medicamento contém menos de 1 mmol de sódio (23 mg) por dose; isto é, é essencialmente “isento de sódio”.
3. Como usar Genotonorm Kabipen
Dosagem recomendada
A dosagem depende da sua superfície corporal, da patologia para a qual está a ser tratado e de como funciona a sua hormona de crescimento. Cada pessoa é diferente. O seu médico indicar-lhe-á a sua dosagem individualizada de Genotonorm Kabipen em miligramas (mg) bem em função do seu peso corporal em quilogramas (kg) ou da sua superfície corporal calculada a partir da sua altura e do seu peso em metros quadrados (m2), assim como o esquema do seu tratamento. Não mude nem a dosagem nem o esquema de tratamento sem consultar o seu médico.
Crianças com deficiência de hormona de crescimento:
0,025-0,035 mg/kg de peso corporal por dia ou 0,7-1,0 mg/m2 de superfície corporal por dia. Podem ser utilizadas dosagens mais altas. Quando a deficiência de hormona de crescimento continua na adolescência, deve continuar o tratamento com Genotonorm Kabipen até que se complete o desenvolvimento físico.
Crianças com síndrome de Turner:
0,045-0,050 mg/kg de peso corporal por dia ou 1,4 mg/m2 de superfície corporal por dia.
Crianças com insuficiência renal crónica:
0,045-0,050 mg/kg de peso corporal por dia ou 1,4 mg/m2 de superfície corporal por dia. Se a velocidade de crescimento for demasiado baixa, pode ser necessário utilizar dosagens mais altas. Pode ser necessário um ajuste de dosagem após 6 meses de tratamento.
Crianças com síndrome de Prader-Willi:
0,035 mg/kg de peso corporal por dia ou 1,0 mg/m2 de superfície corporal por dia. A dosagem diária não deve exceder 2,7 mg. Este tratamento não deve ser utilizado naqueles crianças cuja fase de crescimento tenha praticamente finalizado após a puberdade.
Crianças nascidas pequenas ou com peso mais baixo do que o esperado e com distúrbios do crescimento:
0,035 mg/kg de peso corporal por dia ou 1,0 mg/m2 de superfície corporal por dia. É importante continuar o tratamento até atingir a altura final. O tratamento deve ser suspenso após o primeiro ano se não houver resposta ou se atingir a altura final e o crescimento tiver finalizado.
Adultos com deficiência de hormona de crescimento:
Se continuar a utilizar Genotornorm após o tratamento durante a infância, deve começar com uma dosagem de 0,2-0,5 mg por dia. Esta dosagem deve ser incrementada ou diminuída gradualmente de acordo com os resultados analíticos, assim como com a resposta clínica e os efeitos adversos.
Se a deficiência de hormona de crescimento se inicia durante a idade adulta, deve iniciar com 0,15-0,3 mg por dia. Esta dosagem deve ser incrementada gradualmente em função dos resultados analíticos, assim como da resposta clínica e dos efeitos adversos. A dosagem diária de manutenção raramente excede 1,0 mg por dia. As mulheres podem precisar de dosagens mais altas do que os homens. A dosagem deve ser monitorizada cada 6 meses. Os pacientes com mais de 60 anos devem começar com dosagens de 0,1-0,2 mg por dia e ir incrementando lentamente de acordo com as necessidades individuais. Deve utilizar-se a dosagem mínima eficaz. A dosagem de manutenção raramente excede 0,5 mg por dia. Siga as instruções indicadas pelo seu médico.
Injeção de Genotonorm Kabipen
Este medicamento é utilizado por via subcutânea. Isto significa que é injetado por meio de uma pequena agulha no tecido gordo, justo por baixo da pele. O seu médico ensinar-lhe-á como utilizá-lo. Sempre utilize o medicamento tal como o seu médico lhe indicou. Consulte o seu médico ou farmacêutico se tiver alguma dúvida.
As instruções de uso do dispositivo pré-carregado GoQuick também são fornecidas na caixa do dispositivo pré-carregado.
As instruções para utilizar Genotonorm Kabipen em frasco de dupla câmara junto com Genotonorm Pen são fornecidas no estojo do dispositivo de injeção.
Consulte estas instruções antes de utilizar o seu medicamento.
Quando utilizar um dispositivo pré-carregado ou um dispositivo de injeção Genotonorm Pen, deve colocar a agulha no dispositivo antes de realizar a mistura. Utilize uma agulha nova com cada injeção. As agulhas não devem ser reutilizadas.
- Preparação da injeção:
Pode retirar o medicamento da geladeira meia hora antes da injeção. Isto permite que se atempere um pouco e que a injeção lhe seja mais cómoda.
O dispositivo pré-carregado GoQuick contém um frasco de dupla câmara que tem a hormona de crescimento e o dissolvente líquido. A hormona de crescimento e o dissolvente líquido são misturados ao girar o frasco (ver os passos em detalhe nas Instruções de Uso). Não é necessário nenhum dispositivo adicional.
Genotonorm também é apresentado em frasco de dupla câmara que contém a hormona de crescimento e o dissolvente líquido para utilizar com o dispositivo Genotonorm Pen. A hormona de crescimento e o dissolvente líquido no frasco de dupla câmara podem ser misturados enroscando juntos o dispositivo Genotonorm Pen.
Em ambos os casos, tanto para o dispositivo pré-carregado GoQuick como para o frasco de dupla câmara, dissolva o pó inclinando suavemente até que o pó fique completamente dissolvido.
Quando estiver misturando Genotonorm Kabipen, NÃO AGITE a solução. Misture suavemente. Se agitar a solução, pode fazer com que a hormona de crescimento forme espuma e danifique o medicamento. Observe a solução e não a injete se observar turbidez ou partículas nela.
- Injeção de Genotonorm Kabipen:
Lembre-se de lavar as mãos primeiro e limpar a pele no local da injeção.
Coloque a injeção de hormona de crescimento à mesma hora todos os dias. Um bom momento é a hora de ir para a cama, pois é fácil de lembrar. Também é normal ter um nível mais alto de hormona de crescimento à noite.
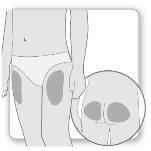
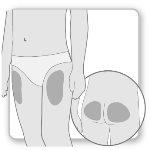
A maior parte dos pacientes utiliza os músculos ou os glúteos para a injeção. Coloque a injeção onde o seu médico lhe ensinou. O tecido gordo da pele pode diminuir de tamanho na zona da injeção. Para evitar isso, mude o ponto da injeção cada vez. Assim, dará tempo à pele e à zona abaixo da pele para se recuperarem entre uma injeção e outra antes de voltar a injetar no mesmo ponto.
Lembre-se de guardar o medicamento na geladeira imediatamente após a injeção.
Se usar mais Genotonorm Kabipen do que deve
Se injetar mais quantidade do que devia, consulte imediatamente o seu médico ou farmacêutico. Os níveis de açúcar no sangue podem descer bruscamente e posteriormente aumentar a níveis demasiado altos. Pode sentir-se agitado, suado, sonolento ou sentir-se estranho e poderia marear-se.
Em caso de sobredosagem ou ingestão acidental, consulte imediatamente o seu médico ou farmacêutico ou ligue para o Serviço de Informação Toxicológica, telefone 91 5620420, indicando o medicamento e a quantidade ingerida.
Se esqueceu de administrar Genotonorm Kabipen
Não se administre uma dose dupla para compensar as doses esquecidas.
É melhor que se injete a hormona de crescimento de forma regular. Se esqueceu de administrar uma dose, coloque a próxima injeção à hora correspondente do dia seguinte. Anote as injeções esquecidas e diga-o ao seu médico na próxima revisão.
Se interromper o tratamento com Genotonorm Kabipen
Consulte o seu médico antes de interromper o tratamento com este medicamento.
Se tiver alguma outra dúvida sobre o uso deste produto, pergunte ao seu médico ou farmacêutico.
4. Efeitos adversos possíveis
Tal como todos os medicamentos, este medicamento pode produzir efeitos adversos, embora nem todas as pessoas os sofram.
Os efeitos adversos frequentes e muito frequentes nos adultos podem começar nos primeiros meses de tratamento e desaparecer de maneira espontânea ou quando se reduz a dose.
Os efeitos adversos muito frequentes (podem afetar mais de 1 de cada 10 doentes) incluem:
Em adultos:
- Dor nas articulações.
- Retenção de líquidos (que se manifesta em forma de dedos inchados ou inchação dos tornozelos).
Os efeitos adversos frequentes (podem afetar até 1 de cada 10 doentes) incluem:
Em crianças:
- Dor nas articulações.
- Verdade, picazón ou dor temporária no local de injeção.
Em adultos:
- Adormecimento/formigamento.
- Dor ou sensação de queimadura nas mãos ou nas axilas (conhecido como síndrome do túnel carpiano).
- Rigidez nos braços e pernas, dor muscular.
Os efeitos adversos pouco frequentes (podem afetar até 1 de cada 100 pessoas) incluem:
Em crianças:
- Leucemia (foi notificada em um pequeno número de doentes com deficiência de hormona de crescimento, alguns dos quais receberam tratamento com somatropina. No entanto, não existe evidência de que a incidência de leucemia esteja aumentada nos receptores de hormona de crescimento sem fatores predisponentes).
- Aumento da pressão intracraniana (que causa sintomas tais como forte dor de cabeça, problemas de visão ou vómitos).
- Adormecimento/formigamento.
- Erupção.
- Picazón.
- Exantema na pele com picazón.
- Dor muscular.
- Aumento do tamanho do peito (ginecomastia).
- Retenção de líquidos (que se manifesta em forma de dedos inchados ou inchação dos tornozelos, durante um curto período de tempo no início do tratamento).
Em adultos:
- Aumento do tamanho do peito (ginecomastia).
Frequência desconhecida: não pode ser estimada a partir dos dados disponíveis:
- Diabetes tipo II.
- Inchação na face.
- Dor de cabeça.
- Diminuição das concentrações da hormona cortisol no sangue.
Em crianças:
- Rigidez nos braços e pernas.
Em adultos:
- Aumento da pressão intracraniana (que causa sintomas tais como forte dor de cabeça, problemas de visão ou vómitos).
- Erupção.
- Picazón.
- Exantema na pele com picazón.
- Verdade, picazón ou dor no local de injeção.
Formação de anticorpos contra a hormona de crescimento injetada, embora isso não pareça afetar a ação da hormona de crescimento.
A pele que há em torno da área de injeção pode tornar-se rugosa e irregular, mas isso não deveria ocorrer se a injeção for realizada em um local diferente cada vez.
O conservante metacresol pode produzir como efeito adverso muito raro a inflamação dos músculos próximos ao local de injeção. Se o seu médico confirmar que desenvolveu este efeito adverso, deveria usar Genotonorm sem metacresol.
Foram relatados casos raros de morte súbita em doentes com síndrome de Prader-Willi. No entanto, não foi possível estabelecer relação entre estes casos e o tratamento com este medicamento.
Se apresentar incômodo ou dor na anca ou joelho enquanto recebe tratamento com Genotonorm, o seu médico pode considerar a possibilidade de que sofra epifisiólise femoral superior ou doença de Legg-Calvé-Perthes.
Outros possíveis efeitos secundários relacionados com o tratamento com hormona de crescimento são os seguintes.
Vous (ou seu filho) pode apresentar aumento dos níveis de açúcar no sangue ou diminuição das concentrações da hormona tiroideia. O seu médico pode realizar testes para determinar e, se necessário, prescrever o tratamento adequado. Ocasionalmente, foi relatada inflamação do pâncreas em doentes tratados com hormona de crescimento.
Comunicação de efeitos adversos
Se experimentar qualquer tipo de efeito adverso, consulte o seu médico, farmacêutico ou enfermeiro, mesmo que se trate de possíveis efeitos adversos que não aparecem neste prospecto. Também pode comunicá-los diretamente através do Sistema Español de Farmacovigilancia de Medicamentos de Uso Humano: https://www.notificaRAM.es.
Ao comunicar efeitos adversos, você pode contribuir para fornecer mais informações sobre a segurança deste medicamento.
5. Conservação de Genotonorm Kabipen
Mantenha fora da vista e do alcance das crianças.
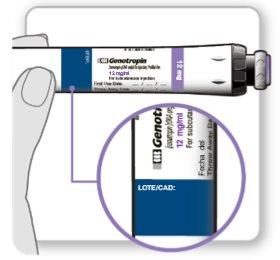
Não utilize este medicamento após a data de validade que aparece no invólucro como MM/AAAA. A data de validade é o último dia do mês que se indica.
Antes da reconstituição
Conservar na geladeira (2°C- 8°C). Conservar o frasco de câmara dupla no embalagem exterior para protegê-lo da luz.
Antes de abri-lo, o medicamento pode ser mantido fora da geladeira durante um período máximo de 1 mês a temperatura não superior a 25°C, mas após este período deve ser descartado.
Depois da reconstituição
Conservar na geladeira (2°C- 8°C) durante um período máximo de 28 dias. Não congelar. Conservar o dispositivo pré-carregado GoQuick no embalagem exterior, ou o frasco de câmara dupla no estojo do dispositivo de injeção, para protegê-lo da luz.
Não utilize este medicamento se observar partículas ou se a solução estiver turva.
Não congele nem exponha este medicamento ao gelo. Se congelar, não o utilize.
Nunca jogue as agulhas ou os frascos vazios na lixeira comum. Quando terminar de utilizar a agulha, deve descartá-la com cuidado em um recipiente especial para agulhas, de forma que ninguém possa utilizá-la ou se picar.
Os medicamentos não devem ser jogados nos esgotos nem na lixeira. Deposite os invólucros e os medicamentos que não precisa no Ponto SIGRE da farmácia. Em caso de dúvida, pergunte ao seu farmacêutico como descartar os invólucros e os medicamentos que não precisa. Dessa forma, ajudará a proteger o meio ambiente.
6. Conteúdo do frasco e informações adicionais
Composição de Genotonorm Kabipen
- O princípio ativo é somatropina*.
- Um frasco contém 5,3 mg ou 12 mg de somatropina*.
- Após a reconstituição, a concentração de somatropina* é 5,3 mg ou 12 mg por ml.
- Os outros componentes do pó são: glicina (E640), manitol (E421), fosfato de sódio anidro (E339) e dihidrogenofosfato de disódio anidro (E339) (ver seção 2 “Genotonorm Kabipen contém sódio”).
- Os ingredientes do solvente são: água para preparações injetáveis, manitol (E421) e metacresol.
*Obtida em células de Escherichia colipor tecnologia de ADN recombinante.
Aspecto de Genotonorm Kabipen e conteúdo do frasco
Pó e solvente para solução para injeção, em um frasco de câmara dupla que contém o pó em uma seção e o solvente na outra (5,3 mg/ml ou 12 mg/ml). O frasco pode vir incluído em um dispositivo pré-carregado. Tamanhos de embalagem: 1 ou 5 dispositivo(s) pré-carregado(s), ou bem 1, 5 ou 20 frasco(s).
Pode ser que apenas alguns tamanhos de embalagens sejam comercializados.
O pó é branco e o solvente transparente.
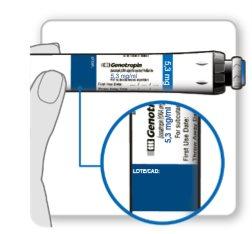
Os frascos devem ser utilizados com um dispositivo de injeção Genotonorm Kabipen específico. Os frascos de Genotonorm Kabipen têm um código de cor, e devem ser utilizados com o dispositivo de injeção Genotonorm Kabipen que coincida com o código de cor, para proporcionar a dose correta: o frasco de Genotonorm Kabipen 5,3 mg (azul) deve ser utilizado com o dispositivo de injeção Genotonorm Kabipen 5,3 (azul). O frasco de Genotonorm Kabipen 12 mg (roxa) deve ser utilizado com o dispositivo de injeção Genotonorm Kabipen 12 (roxa).
As instruções de uso do dispositivo estão incluídas na sua embalagem. Se não tiver um dispositivo de injeção, pode pedi-lo ao seu médico.
Título da autorização de comercialização
Pfizer, S.L.
Avda. de Europa 20 B
Parque Empresarial La Moraleja
28108 Alcobendas (Madrid), Espanha.
Responsável pela fabricação
Pfizer Manufacturing Belgium NV
Rijksweg 12
2870 Puurs-Sint-Amands
Bélgica
Este medicamento está autorizado nos estados membros do Espaço Económico Europeu e no Reino Unido (Irlanda do Norte) com os seguintes nomes:
Genotropin: Áustria, Dinamarca, Finlândia, Alemanha, Grécia, Irlanda, Itália, Holanda, Portugal, Suécia, Reino Unido (Irlanda do Norte).
Genotonorm: Bélgica, França, Luxemburgo.
Genotonorm Kabipen: Espanha.
Data da última revisão deste prospecto:Maio 2024
A informação detalhada deste medicamento está disponível na página web da Agência Espanhola de Medicamentos e Produtos Sanitários (AEMPS) http://www.aemps.gob.es/
INSTRUÇÕES DE USO DE GENOTONORM KABIPEN GOQUICK® Leia estas instruções por completo antes de utilizar o dispositivo GoQuick. Se tiver alguma dúvida sobre a dose ou do tratamento com Genotonorm, ligue para o seu médico ou enfermeiro. Sobre o GoQuick GoQuick é um dispositivo de injeção pré-carregado, multidose e descartável que contém 5,3 mg de somatropina. O dispositivo pode administrar doses de 0,1 mg a 1,5 mg do medicamento. Cada clique da roda negra muda a dose em 0,05 mg. O frasco de Genotonorm incorporado no dispositivo é misturado uma única vez, quando começar a usar um novo dispositivo. Nunca deve trocar o frasco. Quando o dispositivo estiver vazio, deve começar a usar um novo. O dispositivo tem memória de dose. A dose é ajustada cada vez que se vai usar um novo dispositivo. Depois, o dispositivo permite preparar a mesma dose estabelecida em cada injeção. Isso evitará que retire uma dose maior do que a estabelecida. Informação importante
Conservação e eliminação
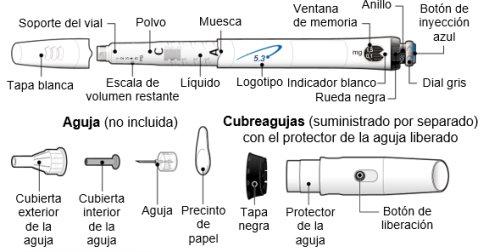
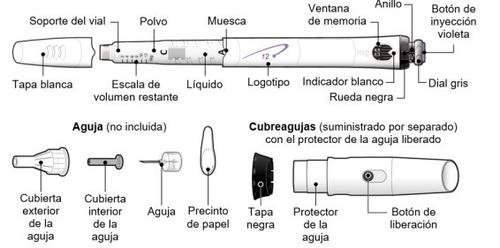
Siga as normas de saúde e segurança locais para descartar (jogar fora) o dispositivo. Pergunte ao seu médico ou enfermeiro se não tiver certeza do que fazer. Partes do dispositivo GoQuick
As agulhas para o dispositivo não estão incluídascom o dispositivo GoQuick. Terá que adquirir agulhas para dispositivos de até 8 mm de comprimento na farmácia.
Preparação e uso de um novo dispositivo GoQuick |
(-:Passo 1.)=100%(Passo 1.:-)(-:Preparação)=89%(Preparação
(-:Empurre a agulha para o suporte do cartucho.)=81%((-:Não aperte demais.)=100%( (-:Deixe ambas as tampas da agulha na agulha.)=0%(<0} |
{0>Passo 2.<}100{>Passo 2.<0}{0>Misture o Genotropin<}0{>Escolha o local de injeção<0}
|
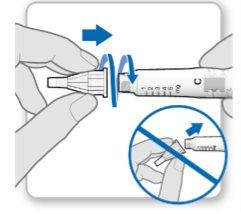
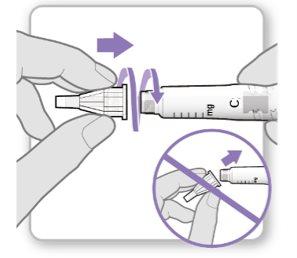
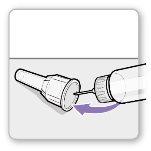
Passo 3.Fixe uma agulha nova
Nota:Tenha cuidado para não fixar a agulha em ângulo. Isso pode causar vazamentos no dispositivo.
|
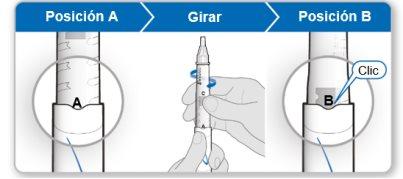
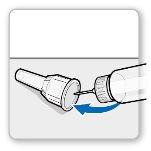
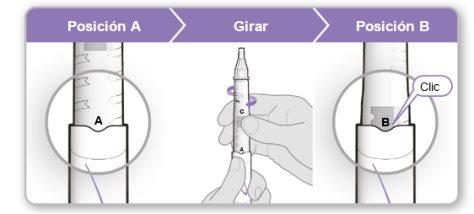
Passo 4.Misture o conteúdo do frasco de Genotonorm
|
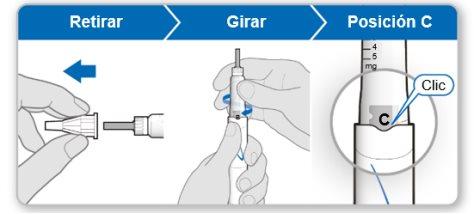
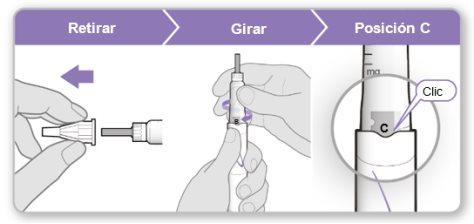
Passo 5.Retire o ar do dispositivo
Nota:Deve ver uma tampa interior da agulha após remover a tampa exterior. Se não vir isso, tente fixar a agulha novamente.
|
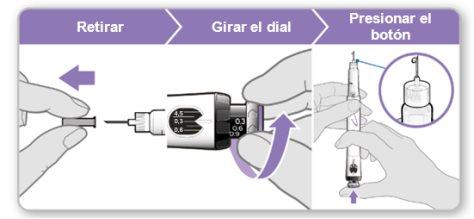
Passo 6.Purgue o dispositivo
A purga elimina o ar restante empurrando uma pequena quantidade de líquido para fora do dispositivo. A dose inicial é de 0,1 mg e é diferente da dose que o seu médico ou enfermeiro prescreveu. Purgue o dispositivo apenas na primeira vez que o utilizar.
Precaução: Nãotoque a agulha para evitar se picar.
|
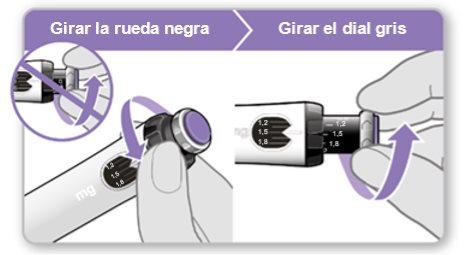
Passo 7.Ajuste e prepare sua dose
A primeira vez que utilizar o dispositivo, ajustará a dose que o seu médico ou enfermeiro prescreveu. Não é necessário que ajuste a dose novamente até que comece a usar um novo dispositivo ou até que o seu médico ou enfermeiro o indique.
Nota:Se não puder girar a roda negra, pressione o botão de injeção azul até que pare de clicar. Depois, tente ajustar a dose novamente. Note que líquido sairá da agulha.
|
Passo 8Verifique sua dose
Sua dose deve estar alinhadacom o indicador branco.
|
Passo 9Administre a injeção de Genotonorm Kabipen
Nota:Se vir uma gota de líquido no local da injeção ou na ponta da agulha, na próxima injeção, tente pressionar o botão de injeção azul por mais tempo antes de retirar a agulha da pele. |
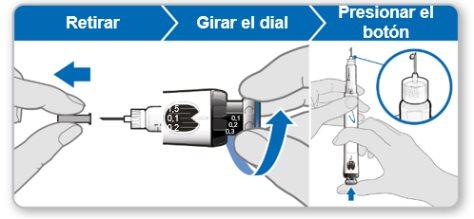
Passo 10Retire a agulha
Conserve o dispositivo na geladeira até a próxima injeção. |
Uso habitual (diário) do dispositivo GoQuick |
Passo 1Preparação
|
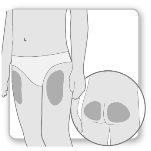
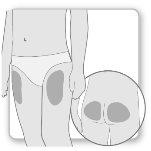
Passo 2Escolha o local de injeção
|
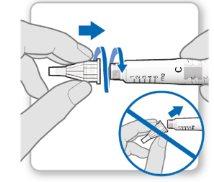
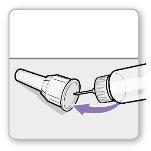
Passo 3Fixe uma agulha nova
|
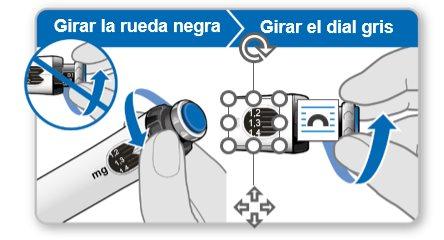
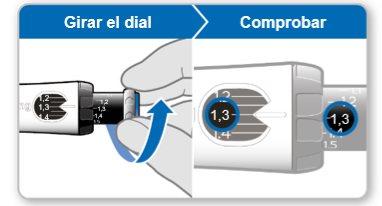
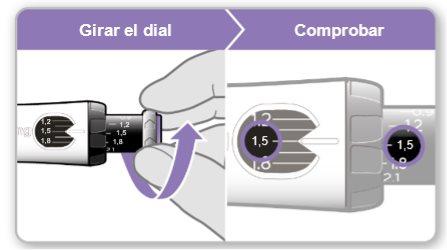
Passo 4Prepare sua dose
|
- Verificarque a dose extraída no anel preto coincide com a dose ajustada na janela de memória.
- Se a dose coincidir, o dispositivo está pronto para administrar a injeção.
Nota:Se a dose a extrair for inferior, o dispositivo não dispõe de uma dose completa de Genotonorm.
Siga as instruções que o seu médico ou enfermeiro lhe tenha dado no caso de não haver uma dose completa no dispositivo. Ou entre em contato com o seu médico ou enfermeiro para obter aconselhamento.
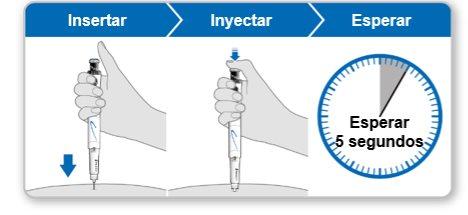
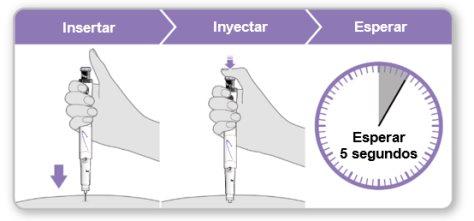
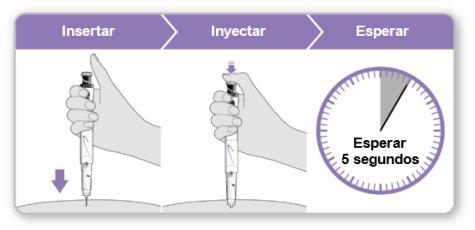
Passo5Administrar a injeção de Genotonorm Kabipen
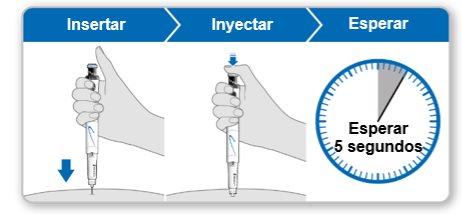
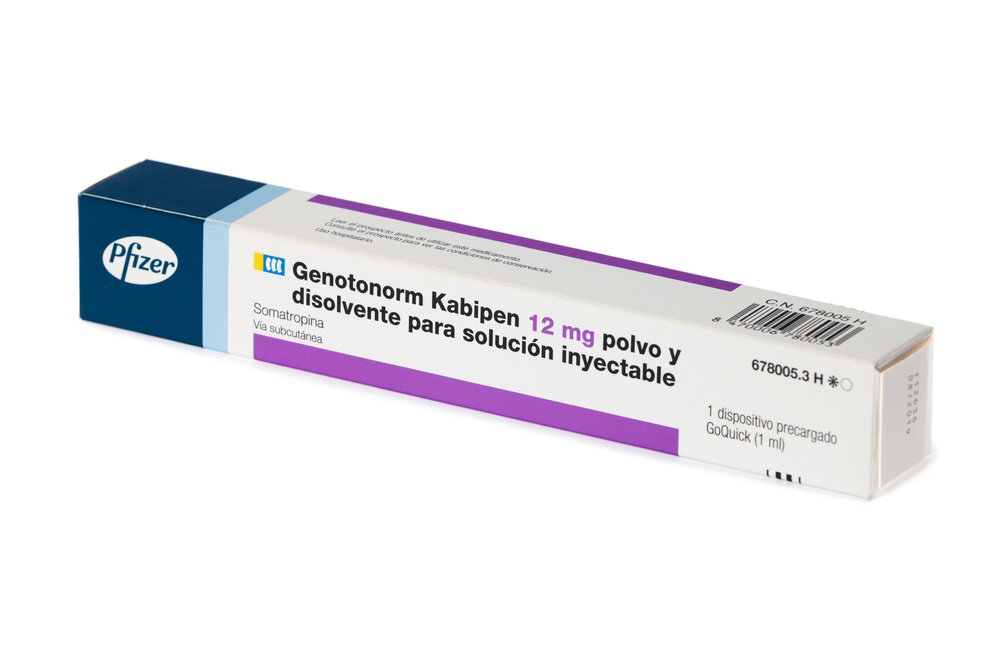
- Seguraro dispositivo sobre o local da injeção.
- Inserira agulha diretamente na pele.
- Pressionaro botão de injeção azul até que deixe de fazer clique.
- Esperar5 segundos completos para garantir que seja injetada a dose completa. Continue pressionando levemente o botão azul de injeção enquanto conta.
- Depois de 5 segundos, retire a agulha da sua pele em linha reta.
Nota:Se você vir uma gota de líquido no local da injeção ou na ponta da agulha, na próxima injeção, tente pressionar o botão de injeção azul por mais tempo antes de retirar a agulha da pele.
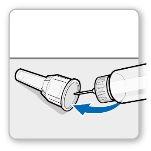
Passo6Retirar a agulha
|
Precaução: Nãotoque a agulha para evitar se picar.
|
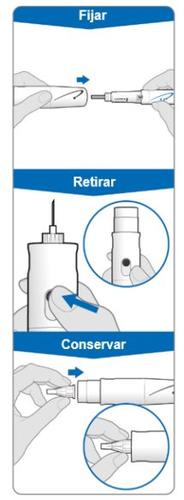 Uso da capa da agulha (opcional)
Uso da capa da agulha (opcional)
A capa da agulha é um artigo opcional que é fornecido separadamente para ocultar a agulha durante a injeção.
Fixar a capa da agulha:
Fixar a capa da agulha após o passo 5 (Ajuste e uso de um novo dispositivo GoQuick) para evitar se picar.
- Retirar a tampa preta da capa da agulha.
- Se o protetor da agulha se deslizar para fora, empurre-o para dentro da capa da agulha até que encaixe no lugar.
- Alinear o logotipo preto da capa da agulha com o logotipo azul do dispositivo. Empurre com cuidado a capa da agulha no dispositivo até que encaixe no lugar.
- Após o passo 6 (Preparação e uso de um novo dispositivo GoQuick), pressione o botão preto para liberar o protetor da capa da agulha.
- Siga as instruções descritas no passo 7 (Preparação e uso de um novo dispositivo GoQuick).
Para retirar a agulha com a capa da agulha colocada:
- Colocar a capa exterior da agulha no extremo da capa da agulha.
- Utilizar a capa exterior da agulha para empurrar a capa da agulha até que encaixe no lugar.
- Utilizar a capa da agulha para desenroscar a agulha e descartar (jogar) em um recipiente para objetos perfurantes adequado.
- Deixar a capa da agulha no dispositivo.
- Colocar a tampa preta na capa da agulha. Conservar o dispositivo na geladeira.
Para retirar a capa da agulha:
- Retirar primeiro a agulha e, em seguida, retire suavemente a capa da agulha do dispositivo.
- Nãodescarte a capa da agulha. Ela pode ser usada com o seu próximo dispositivo.
INSTRUÇÕES DE USO DE GENOTONORM KABIPEN GOQUICK® |
Leia estas instruções por completo antes de usar o dispositivo GoQuick. Se tiver alguma dúvida sobre a dose ou o tratamento com Genotonorm Kabipen, ligue para o seu médico ou enfermeiro. Sobre o GoQuick GoQuick é um dispositivo de injeção pré-carregado, multidose e descartável que contém 12 mg de somatropina. O dispositivo pode administrar doses de 0,3 mg a 4,5 mg de Genotonorm Kabipen. Cada clique da roda preta altera a dose em 0,15 mg. O frasco de Genotonorm incorporado no dispositivo é misturado uma única vez, quando você começar a usar um dispositivo novo. Nunca deve trocar o frasco. Quando o dispositivo estiver vazio, você deve começar a usar um novo. O dispositivo tem memória de dose. A dose é ajustada cada vez que você vai usar um novo dispositivo. Depois, o dispositivo permite preparar a mesma dose estabelecida em cada injeção. Isso evitará que você extraia uma dose maior do que a estabelecida. Informação importante
Conservação e eliminação
|
Partes do dispositivo GoQuick
As agulhas para dispositivos não estão incluídascom o dispositivo GoQuick. Você precisará adquirir agulhas para dispositivos de até 8 mm de comprimento na farmácia.
|
Preparação e uso de um novo dispositivo GoQuick |
Passo 1Preparação
Passo2Escolher o local da injeção
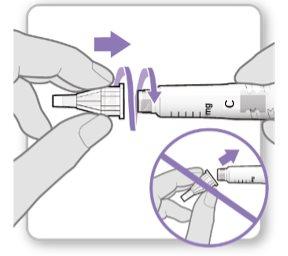
Passo3Fixar uma agulha nova
Nota:Tenha cuidado para não fixar a agulha em ângulo. Isso pode causar vazamentos no dispositivo.
|
Passo4.Misturar o conteúdo do frasco de Genotonorm
| |
Passo5Retirar o ar do dispositivo
Nota:Você deve ver uma capa interior da agulha após retirar a capa exterior. Se não vir isso, tente fixar a agulha novamente.
| |
Passo6Purgar o dispositivo
A purga remove o ar restante empurrando uma pequena quantidade de líquido para fora do dispositivo. A dose inicial é de 0,3 mg e é diferente da dose que o seu médico ou enfermeiro prescreveu. Purgue o dispositivo apenas na primeira vez que o usar.
Precaução: Nãotoque a agulha para evitar se picar.
| |
Passo7Ajustar e preparar sua dose
A primeira vez que usar o dispositivo, você ajustará a dose que o seu médico ou enfermeiro prescreveu. Não é necessário ajustar a dose novamente até que comece a usar um novo dispositivo ou até que o seu médico ou enfermeiro o indique.
Nota: Se não conseguir girar a roda preta, pressione o botão de injeção violeta até que deixe de fazer clique. Depois, tente ajustar a sua dose novamente. Note que líquido sairá da agulha.
| |
Passo8Verificar sua dose
Sua dose deve estar alinhadacom o indicador branco.
| |
Passo9Administrar a injeção de Genotonorm Kabipen
Nota:Se você vir uma gota de líquido no local da injeção ou na ponta da agulha, na próxima injeção, tente pressionar o botão de injeção violeta por mais tempo antes de retirar a agulha da pele. | |
Passo10Retirar a agulha
| |
Uso habitual (diário) do dispositivo GoQuick | |
Passo1Preparação
| |
Passo2Escolher o local da injeção
Passo3Fixar uma agulha nova o3Fixar uma agulha nova
Nota:Tenha cuidado para não fixar a agulha em ângulo. Isso pode causar vazamentos no dispositivo.
| |
Paso4Preparar sua dose
| |
Nota:Se a dose a extrair for inferior, o dispositivo não dispõe de uma dose completa de Genotonorm. Siga as instruções que seu médico ou enfermeiro lhe deu no caso de não haver uma dose completa no dispositivo. Ou comunique-se com seu médico ou enfermeiro para obter aconselhamento. | |
Paso5Administrar a injeção de Genotonorm Kabipen
Nota:Se você vir uma gota de líquido no local da injeção ou na ponta da agulha, com a próxima injeção, tente pressionar o botão de injeção violeta por mais tempo antes de sacar a agulha da pele. | |
Paso6Retirar a agulha
| |
Precaução: Nãotoque a agulha para evitar se picar.
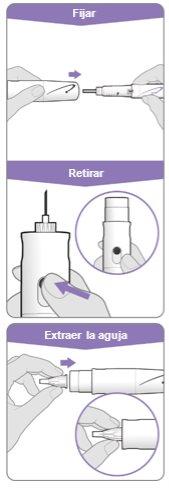
Uso do cobreagulha (opcional) O cobreagulha é um artigo opcional que é fornecido separadamente para ocultar a agulha durante a injeção.
Fixar o cobreagulha após o passo 5 (Ajuste e uso de um novo dispositivo GoQuick) para evitar se picar.
Para retirar a agulha com o cobreagulha colocado:
Para retirar o cobreagulha:
|
- País de registo
- Forma farmacêuticaINJETÁVEL, 12 mg de somatropina
- Código ATCH01AC01
- Substância ativa
- Requer receita médicaSim
- Fabricante
- Esta informação é apenas para fins informativos e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento.
- Alternativas a GENOTONORM KABIPEN 12 mg PÓ E SOLVENTE PARA SOLUÇÃO INJETÁVELForma farmacêutica: INJETÁVEL, 5,3 mg de somatropinaSubstância ativa: somatropinFabricante: Pfizer S.L.Requer receita médicaForma farmacêutica: INJETÁVEL, 0,2 mg de somatropinaSubstância ativa: somatropinFabricante: Pfizer S.L.Requer receita médicaForma farmacêutica: INJETÁVEL, 0,4 mg de somatropinaSubstância ativa: somatropinFabricante: Pfizer S.L.Requer receita médica
Médicos online para GENOTONORM KABIPEN 12 mg PÓ E SOLVENTE PARA SOLUÇÃO INJETÁVEL
Avaliação de dosagem, efeitos secundários, interações, contraindicações e renovação de receita para GENOTONORM KABIPEN 12 mg PÓ E SOLVENTE PARA SOLUÇÃO INJETÁVEL — sujeita a avaliação médica e à regulamentação local.
Obtenha uma receita de GENOTONORM KABIPEN 12 mg PÓ E SOLVENTE PARA SOLUÇÃO INJETÁVEL online
Preencha um formulário de 2 minutos
Conte-nos os seus sintomas, historial e o medicamento que está a solicitar.
Escolha um médico ou deixe-nos atribuir
Escolha um especialista ou ligamos com o próximo médico disponível.
O médico analisa o seu caso
Normalmente em 30 minutos. Pode fazer perguntas adicionais por chat.
Levante em qualquer farmácia
Receita eletrónica enviada para o seu e-mail — válida em toda a Espanha.
Perguntas frequentes

Receba atualizações e ofertas exclusivas
Seja o primeiro a conhecer novos serviços, atualizações do marketplace e ofertas exclusivas para subscritores.





 Fixar o cobreagulha:
Fixar o cobreagulha:


