PHOXILIUM 1,2 mmol/L SOLUÇÃO DE FOSFATO PARA HEMODIÁLISE/HEMOFILTRAÇÃO


Como utilizar PHOXILIUM 1,2 mmol/L SOLUÇÃO DE FOSFATO PARA HEMODIÁLISE/HEMOFILTRAÇÃO
Traduzido com IA
Esta informação é fornecida apenas para fins informativos e não substitui a consulta de um médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
Mostrar traduçãoConteúdo do folheto informativo
Introducción
Prospecto: información para el usuario
PHOXILIUM® 1,2 mmol/l de fosfato
Solución para hemodiálisis y hemofiltración
Cloruro cálcico dihidratado, cloruro magnésico hexahidratado, cloruro sódico, bicarbonato de sodio, cloruro potásico, fosfato disódico dihidratado
Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque contiene información importante para usted.
- Conserve este prospecto, ya que puede tener que volver a leerlo.
- Si tiene alguna duda, consulte a su médico, farmacéutico o enfermero.
- Si experimenta efectos adversos, consulte a su médico, farmacéutico o enfermero, incluso si se trata de efectos adversos que no aparecen en este prospecto. Ver sección 4.
Contenido del prospecto
- Qué es Phoxilium y para qué se utiliza
- Qué necesita saber antes de recibir Phoxilium
- Cómo usar Phoxilium
- Posibles efectos adversos
- Conservación de Phoxilium
- Contenido del envase e información adicional
1. Qué es Phoxilium y para qué se utiliza
Phoxilium, que pertenece al grupo de soluciones de hemofiltrados, contiene cloruro cálcico dihidratado, cloruro magnésico hexahidratado, cloruro sódico, bicarbonato sódico, cloruro potásico y fosfato disódico dihidratado.
Phoxilium se utiliza en hospitales en tratamientos de cuidados intensivos para corregir los desequilibrios químicos en el sangre causados por una lesión renal.
El objetivo de estos tratamientos, que incluyen terapia de sustitución renal, es eliminar de la sangre los productos de desecho que se acumulan cuando los riñones no funcionan bien.
La solución Phoxiliumse utiliza especialmente en el tratamiento de pacientes en estado crítico con una lesión renal aguda y que además presentan:
- una concentración normal de potasio en sangre (caliemia normal), o bien
- una concentración normal o baja de fosfato en sangre (fosfatemia normal o hipofosfatemia).
Este medicamento también puede utilizarse en caso de intoxicación por medicamentos, sustancias dializables o filtrables.
2. Qué necesita saber antes de usar Phoxilium
No utilizar Phoxilium en los tres casos siguientes:
- una concentración alta de potasio en sangre (hipercaliemia)
- una concentración alta de bicarbonato en sangre (alcalosis metabólica)
- una concentración alta de fosfato en sangre (hiperfosfatemia)
No someter al paciente a hemodiálisis ni hemofiltración en los tres casos descritos a
continuación:
- Si la hemofiltración no puede corregir los síntomas causados por una concentración elevada de
urea en sangre (síntomas urémicos)como consecuencia de una lesión renal con
hipercatabolismo acusado (un aumento anormal del proceso de degradación de sustancias).
- Si la presión arterial en el acceso vascular es insuficiente.
- Si la capacidad de coagulación sanguínea es reducida (anticoagulación sistémica) y existe
riesgo elevado de que se produzca una hemorragia.
Advertencias y precauciones
Consulte a su médico, farmacéutico o enfermero antes de empezar a usar Phoxilium.
La condición de su sangre se comprobará antes y durante el tratamiento. Se controlará, por
ejemplo, el equilibrio acidobásico y la concentración de sales en la sangre (electrolitos), incluidas todas las entradas (perfusión intravenosa) y salidas (diuresis) de líquidos, incluso las que no estén relacionadas directamente con el tratamiento.
Uso de Phoxilium con otros medicamentos
Comunique a su médico o farmacéutico si está utilizando, ha utilizado recientemente o podría
tener que utilizar cualquier otro medicamento. Debe hacerlo porque la concentración de algunos
medicamentos puede afectar al tratamiento con Phoxilium. Su médico decidirá si es preciso
modificar la dosis de los medicamentos que utiliza.
En concreto, hable con su médico si toma alguno de los medicamentos siguientes:
- Suplementos de fosfato (por ejemplo, líquidos nutritivos), ya que pueden aumentar el riesgo de
concentración alta de fosfato en sangre (hiperfosfatemia).
- Vitamina D y medicamentos que contengan cloruro de calcio o gluconato de calcio, ya que pueden aumentar el riesgo de concentración alta de calcio en sangre (hipercalcemia).
- Bicarbonato de sodio, ya que puede provocar un aumento del riesgo de que exista exceso de
bases en la sangre (alcalosis metabólica).
- Citrato usado como anticoagulante, ya que puede reducir los niveles de calcio en el plasma.
Embarazo, lactancia y fertilidad
Embarazo y lactancia:
No hay datos clínicos documentados sobre el uso de
este medicamento durante el embarazo y la lactancia. Este medicamento solo debe administrarse a mujeres embarazadas y en periodo de lactancia si es claramente necesario.
Fertilidad:
No se prevé ningún efecto en la fertilidad, dado que el calcio, el sodio, el potasio, el magnesio, el cloruro, el hidrogenofosfato y el bicarbonato son componentes normales del organismo.
Conducción y uso de máquinas
Phoxilium no afecta a la capacidad para conducir vehículos o manejar maquinaria.
3. Cómo usar Phoxilium
Phoxilium es un producto de uso hospitalario que sólo debe ser administrado por profesionales
médicos. El volumen de Phoxilium empleado y, por lo tanto, la dosis, dependerá de sus
condiciones. El volumen de dosis será determinado por el médico responsable del tratamiento.
Phoxilium puede administrarse directamente en la corriente sanguínea (vía intravenosa) mediante un aparato de TCRR o mediante hemodiálisis, una técnica en la que la solución circula por un lado de la membrana de
diálisis mientras la sangre lo hace por el otro.
Siga exactamente las instrucciones de administración del medicamento
contenidas en este prospecto o las indicadas por su médico, farmacéutico o enfermero. En caso de duda, pregunte a su médico, farmacéutico o enfermero.
Para obtener instrucciones de uso, consulte el apartado “Esta información está destinada
únicamente a profesionales del sector sanitario”.
Si usa más Phoxilium del que debe
Phoxilium es un producto de uso hospitalario que es administrado únicamente por profesionales
médicos; además, se lleva a cabo un control exhaustivo del equilibrio de líquidos, así como
analíticas sanguíneas.
Por lo tanto, es improbable que use más Phoxilium del que debe.
En el caso improbable de que se produzca una sobredosis, el médico adoptará las medidas
correctivas necesarias y ajustará la dosis.
La sobredosis puede derivar en una sobrecarga de líquidos, en una reducción de la concentración de bicarbonato en el plasma (acidosis metabólica) y/o en una concentración elevada de fosfato (hiperfosfatemia) si el paciente tiene una lesión renal. Podría tener consecuencias muy graves, como insuficiencia cardiaca
congestiva o alteraciones en sus análisis de sangre.
Si tiene cualquier otra duda sobre el uso de este medicamento, pregunte a su médico o
farmacéutico.
4. Posibles efectos adversos
Al igual que todos los medicamentos, este medicamento puede producir efectos adversos,
aunque no todos las personas los sufran.
Es posible que el paciente experimente los tres efectos secundarios relacionados con el uso de
Phoxiliumque se describen a continuación:
- Volumen de agua en el cuerpo anormalmente elevado o reducido (hiper o hipovolemia)
- Variaciones en los niveles de sales en la sangre (desequilibrios electrolíticos, como hiperfosfatemia)
- Aumento de la concentración de bicarbonato en plasma (alcalosis metabólica) o reducción de la concentración de bicarbonato en el plasma (acidosis metabólica).
Existen además algunos efectos secundariosque pueden deberse a los tratamientos de diálisis, por ejemplo:
- Nauseas, vómitos, calambres musculares y presión arterial baja (hipotensión).
Comunicación de efectos adversos
Si experimenta cualquier tipo de efecto adverso, consulte a su médico, farmacéutico o
enfermero, incluso si se trata de posibles efectos adversos que no aparecen en este prospecto.
También puede comunicarlos directamente a través del Sistema Español de Farmacovigilancia
de Medicamentos de Uso Humano: www.notificaRAM.es. Mediante la comunicación de efectos
adversos usted puede contribuir a proporcionar más información sobre la seguridad de este
medicamento.
5. Conservación de Phoxilium
Mantener este medicamento fuera de la vista y del alcance de los niños.
No utilice este medicamento después de la fecha de caducidad que aparece en la etiqueta y en el
envase. La fecha de caducidad es el último día del mes que se indica.
Conservar a una temperatura entre 4°C y 30°C. No refrigerar o congelar.
Se ha demostrado la estabilidad física y química en uso de la solución reconstituida durante 24 horas a 22°C. De no utilizar la solución inmediatamente, las condiciones y el tiempo de almacenamiento serán responsabilidad del usuario; en cualquier caso, este tiempo no debe ser superior a 24 horas, incluida la duración del tratamiento.
No utilizar este medicamento si la solución está turbia o si el envoltorio presenta algún daño.
Todos los precintos deben estar intactos.
Los medicamentos no se deben tirar por los desagües ni a la basura. Pregunte a su farmacéutico
cómo deshacerse de los envases y de los medicamentos que ya no necesita. De esta forma,
ayudará a proteger el medio ambiente.
6. Contenido del envase e información adicional
PHOXILIUM ES PL POLIOLEFINA CON CONECTOR LUER CON VÁLVULA; 2016-07
Composición de Phoxilium
A continuación se enumeran los principios activos antes y después de la mezcla (reconstitución) de la solución.
Los principios activos antes de la mezcla son:
1.000 ml de solución del compartimento pequeño (A)contienen:
Cloruro cálcico, 2 H2O 3,68 g
Cloruro magnésico, 6 H2O 2,44 g
1.000 ml de solución del compartimento grande (B)contienen:
Cloruro sódico 6,44 g
Bicarbonato de sodio 2,92 g
Cloruro potásico 0,314 g
Fosfato disódico, 2 H2O 0,225 g
Los principios activos después de la mezcla son:
Las soluciones de los compartimentos A (250 ml) y B (4.750 ml) se mezclan para producir una solución reconstituida (5.000 ml) cuya composición es la siguiente:
mmol/l
Calcio, Ca2+ 1,25
Magnesio, Mg2+ 0,6
Sodio, Na+ 140
Cloruro, Cl- 115,9
Hidrógeno fosfato, HPO42- 1,2
Bicarbonato, HCO3- 30
Potasio, K+ 4
Osmolaridad teórica: 293 mOsm/l
Los demás componentes son:
- Dióxido de carbono (para ajuste de pH) E290
- Ácido clorhídrico (para ajuste de pH) E507
- Agua para preparaciones inyectables
Aspecto del producto y contenido del envase
Phoxilium es una solución para hemodiálisis y hemofiltración que se presenta en una bolsa que consta de dos compartimentos. La solución final reconstituida se obtiene tras romper el sello hermético y mezclar ambas soluciones. La solución reconstituida es transparente e incolora. Cada bolsa (A+B) contiene 5.000 ml de solución para hemodiálisis y hemofiltración. La bolsa está envuelta en película transparente.
Cada caja contiene dos bolsas y un prospecto.
Titular de la autorización de comercialización y responsable de la fabricación:
Vantive Belgium SRL
Boulevard d´Angleterre 2
1420 Braine-l´Alleud
Bélgica
Fabricante:
BIEFFE MEDITAL S.P.A.
Via Stelvio 94,
23035 Sondalo (SO)
ITALIA
O
Vantive Manufacturing Limited
Moneen Road,
Castlebar, County Mayo, F23 XR63
Irlanda
Pueden solicitar más información respecto a este medicamento dirigiéndose al representante local del titular de la autorización de comercialización:
Vantive Health, S.L.
Polígono Industrial Sector 14.
C/ Pouet de Camilo, 2
46394 Ribarroja del Turia (Valencia)
España
Este medicamento está autorizado en los estados miembros del Espacio Económico Europeo y en el Reino Unido (Irlanda del Norte) con los siguientes nombres:
Alemania, Austria, Bélgica, Bulgaria, Chipre, Dinamarca, Eslovaquia, Eslovenia, España,
Estonia, Finlandia, Francia, Grecia, Islandia, Irlanda, Italia, Letonia, Lituania, Luxemburgo,
Malta, Noruega, Países Bajos, Polonia, Portugal, Reino Unido (Irlanda del Norte), Rumanía y Suecia: Phoxilium
Hungría: Phoxil
Fecha de la última revisión de este prospecto:
10/2018
La información detallada y actualizada de este medicamento está disponible en la página Web de la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS) http://www.aemps.es
--------------------------------------------------------------------------------------------------------------------
Esta información está destinada únicamente a profesionales del sector sanitario
Phoxilium 1,2 mmol/l de fosfato
Solución para hemodiálisis y hemofiltración
Precauciones
Debe seguir con exactitud las instrucciones de uso y manipulaciónde Phoxilium.
Las soluciones de los dos compartimentos debenmezclarse antes de usarse.
El uso de una solución contaminada puede causar sepsis y shock.
Para aumentar la comodidad del paciente, se puede calentar Phoxilium hasta alcanzar los 37°C. El calentamiento previo al uso de la solución se debe realizar antes de la reconstitución utilizando solo calor seco. Las soluciones no se deben calentar en agua ni en un horno microondas. Antes de la administración, se debe comprobar visualmente que Phoxilium no contenga partículas ni haya perdido el color original. No administre la solución a menos que ésta sea transparente y el precinto esté intacto.
La concentración de fosfato inorgánico debe determinarse periódicamente. El fosfato inorgánico
debe sustituirse en aquellos casos en los que el nivel de fosfato en sangre sea bajo.
La adición de bicarbonato sódico de sustitución puede aumentar el riesgo de alcalosis metabólica.
En caso de desequilibrio de líquidos, se debe supervisar minuciosamente la situación clínica y
restaurar el equilibro de líquidos:
- En caso de hipervolemia, la velocidad de ultrafiltración neta prescrita para el dispositivo de TCRR puede aumentarse y/o la velocidad de administración de aquellas soluciones distintas de los líquidos de rehidratación y/o el líquido de diálisis puede reducirse.
- En caso de hipovolemia, la velocidad de la ultrafiltración neta prescrita para el dispositivo de TCRR puede reducirse y/o la velocidad de administración de aquellas soluciones distintas de los líquidos de rehidratación y/o el líquido de diálisis puede aumentarse.
Advertencias:
Phoxilium no se debe utilizar en pacientes con hiperpotasemia. Se debe supervisar la concentración de potasio en el suero antes y durante la hemofiltración y/o la hemodiálisis.
Phoxilium es una solución que contiene potasio, por lo que puede provocar hiperpotasemia transitoria una vez iniciado el tratamiento. En tal caso, reduzca la velocidad de perfusión y asegúrese de que se haya alcanzado la concentración de potasio necesaria. Si la hiperpotasemia no remite, suspenda el tratamiento de inmediato.
Si se produce hiperpotasemia cuando se usa Phoxilium como líquido de diálisis, puede ser necesario administrar un líquido de diálisis sin potasio para aumentar la velocidad de eliminación del potasio.
Debido a que Phoxilium es una solución que contiene fosfato, puede provocar hiperfosfatemia temporal una vez iniciado el tratamiento. En tal caso, se debe reducir la velocidad de perfusión hasta alcanzar la concentración de fosfato deseada. Si la hiperfosfatemia no remite, la administración debe suspenderse de inmediato.
Los electrolitos y los parámetros ácido-básicos en sangre deben controlarse periódicamente en los pacientes tratados con Phoxilium. Phoxilium contiene hidrógeno fosfato, un ácido débil que puede afectar al equilibrio acidobásico del paciente. Si durante el tratamiento con Phoxilium aparece acidosis metabólica o esta empeora, es posible que sea necesario reducir la velocidad de perfusión o suspender la administración.
Phoxilium no contiene glucosa, por lo que su administración puede provocar hipoglucemia. Los niveles de glucosa en la sangre se deben supervisar con regularidad en los pacientes diabéticos (incluida una consideración minuciosa en el caso de los pacientes que tomen insulina u otros medicamentos hipoglucemiantes), pero también se deben tener en cuenta en los pacientes no diabéticos, debido, por ejemplo, al riesgo de hipoglucemia asintomática durante el procedimiento. Si se produce una hipoglucemia, se debe considerar el uso de una solución con glucosa. Pueden ser necesarias otras medidas correctoras para mantener el control glucémico deseado.
Posología:
El volumen y la velocidad a la que se administra Phoxilium dependen de la concentración de fosfato y otros electrolitos en la sangre, del equilibrio ácido-básico, del equilibrio de líquidos y del estado clínico general del paciente. El volumen de la solución de sustitución y/o del líquido de diálisis que se debe administrar también dependerá de la intensidad (dosis) del tratamiento deseada. La pauta de administración (dosis, velocidad de la perfusión y volumen acumulado) de Phoxilium solo debe determinarla un médico con experiencia en medicina intensiva y TCRR (terapia continua de reemplazo renal).
Por tanto, el volumen de la dosis lo determinará y prescribirá el médico responsable.
La velocidad de flujo de la solución de sustitución en terapias de hemofiltración y hemodiafiltración es:
Adultos: 500-3.000 ml/h
La velocidad de flujo del líquido de diálisis en terapias de hemodiálisis y hemodiafiltración continua es:
Adultos: 500-2.500 ml/h
La velocidad de flujo total combinada utilizada habitualmente para la TCRR (líquido de diálisis y soluciones de sustitución) en adultos es de 2.000 a 2.500 ml/h aproximadamente, lo que corresponde a un volumen de líquido diario aproximado de entre 48 y 60 l.
Población pediátrica:
En el caso de los niños, desde neonatos hasta adolescentes de hasta 18 años, el intervalo de velocidad de flujo cuando se utiliza como solución de sustitución en hemofiltración y hemodiafiltración y como solución de diálisis (líquido de diálisis) en hemodiálisis continua y hemodiafiltración continua es de 1.000 a 4.000 ml/h/1,73 m2.
En los adolescentes (de 12 a 18 años), cuando se calcule que la dosis pediátrica supera la dosis máxima para adultos, se debe utilizar la dosis recomendada para adultos.
Instrucciones de uso y manipulación
La solución del compartimento pequeño A se añade a la solución del compartimento grande B tras romper el sello hermético e inmediatamente antes de utilizarse. La solución reconstituida debe ser transparente e incolora.
Se debe emplear una técnica aséptica durante la manipulación y administración al paciente.
Utilizar solamente si el envoltorio está íntegro, los precintos están intactos, el sello despegable no está roto y la solución es transparente. Apriete la bolsa para asegurarse de que no haya fugas. Si se descubre alguna fuga, deseche la solución inmediatamente ya que no se puede garantizar su esterilidad.
El compartimento grande B tiene un acceso de inyección para añadir otros fármacos que seannecesarios una vez reconstituida la solución.Es responsabilidad del médico juzgar la compatibilidad de la medicación añadida a la solución Phoxilium comprobando el cambio eventual de color y/o precipitación, complejos insolubles o cristales. Antes de añadir un medicamento, compruebe que sea soluble y estable en este medicamento y que el intervalo de pH de Phoxilium es adecuado (el intervalo de pH de la solución reconstituida es 7,0-8,5). Los aditivos podrían no ser compatibles. Se deben consultar las instrucciones de uso del medicamento que se va a añadir.
Retire cualquier líquido del acceso de inyección, sujete la bolsa en posición vertical hacia abajo,
añada el fármaco a través del puerto de inyección y mezcle completamente. La introducción y el mezclado de los aditivos siempre debe realizarse antes de conectar la bolsa de la solución al circuito estracorpóreo. La solución debe administrarse inmediatamente.
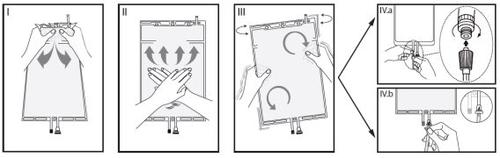
IRetire el envoltorio de la bolsa inmediatamente antes de usarla y deseche los demás materiales
de embalaje. Rompa el sello hermético sujetando el compartimento pequeño entre las dos manos y apretando hasta que se abra la pared que separa ambos compartimentos (vea la figura I que aparece abajo).
IIPresione el compartimento grande con ambas manos hasta que la pared entre los dos
compartimentos esté totalmente abierta (vea la figura II que aparece abajo).
IIIAsegúrese de que las soluciones se mezclan completamente agitando la bolsa suavemente. La solución ya está lista para su uso y la bolsa puede colgarse en el equipo (vea la figura III que
parece abajo).
IVLa línea de líquido de diálisis o de sustitución puede conectarse a cualquiera de los dos
conectores de acceso.
IV.aSi se utiliza el conector luer, quite el tapón con un movimiento de giro y extracción y conecte el conector luer macho de la línea de diálisis o sustitución en el receptor luer hembra de la bolsa mediante un movimiento empuje y giro. Asegúrese de que la conexión está bien hecha y apretada. La conexión se abrirá. Compruebe que el líquido circula libremente. (vea la figura IV.a que aparece abajo).
Si la línea de diálisis o sustitución se desconecta del conector luer, el conector se cerrará y el flujo de la solución se detendrá. El puerto luer es un puerto sin aguja que se puede limpiar.
IV.bSi se utiliza el acceso de inyección, retire antes el tapón levantándolo. El puerto de inyección es un puerto que se puede desinfectar con torunda. Introduzca después
el espigón a través de la pared de goma. Compruebe que el líquido circula libremente (vea la
figura IV.b que aparece abajo)
La solución reconstituida debe utilizarse inmediatamente. En caso de no utilizarla inmediatamente, tenga en cuenta que la solución reconstituida debe utilizarse en el plazo de las 24 horas posteriores a la adición de la solución A a la solución B, incluida la duración del tratamiento.
La solución reconstituida es para un solo uso. Deseche la solución sobrante inmediatamente
después del uso.
La eliminación del medicamento no utilizado y de todos los materiales que hayan estado en contacto con él, se realizará de acuerdo con la normativa local.
PHOXILIUM ES PVC CONECTOR LUER CON VÁSTAGO; 2016-07
Composición de Phoxilium
A continuación se enumeran los principios activos antes y después de la mezcla (reconstitución) de la solución.
Los principios activos antes de la mezcla son:
1.000 ml de solución del compartimento pequeño (A)contienen:
Cloruro cálcico, 2 H2O 3,68 g
Cloruro magnésico, 6 H2O 2,44 g
1.000 ml de solución del compartimento grande (B)contienen:
Cloruro sódico 6,44 g
Bicarbonato de sodio 2,92 g
Cloruro potásico 0,314 g
Fosfato disódico, 2 H2O 0,225 g
Los principios activos después de la mezcla son:
Las soluciones de los compartimentos A (250 ml) y B (4.750 ml) se mezclan para producir una solución reconstituida (5.000 ml) cuya composición es la siguiente:
mmol/l
Calcio, Ca2+ 1,25
Magnesio, Mg2+ 0,6
Sodio, Na+ 140
Cloruro, Cl- 115,9
Hidrógeno fosfato, HPO42- 1,2
Bicarbonato, HCO3- 30
Potasio, K+ 4
Osmolaridad teórica: 293 mOsm/l
Los demás componentes son:
Dióxido de carbono (para ajuste de pH) E290
Ácido clorhídrico (para ajuste de pH) E507
Agua para preparaciones inyectables
Aspecto del producto y contenido del envase
Phoxilium es una solución para hemodiálisis y hemofiltración que se presenta en una bolsa que consta de dos compartimentos. La solución final reconstituida se obtiene tras romper el vástago rompible y mezclar ambas soluciones. La solución reconstituida es transparente e incolora. Cada bolsa (A+B) contiene 5.000 ml de solución para hemodiálisis y hemofiltración. La bolsa está envuelta en película transparente.
Cada caja contiene dos bolsas y un prospecto.
Titular de la autorización de comercialización y responsable de la fabricación:
Vantive Belgium SRL
Boulevard d´Angleterre 2
1420 Braine-l´Alleud
Bélgica
Fabricante:
Bieffe Medital S.p.A
Via Stelvio 94
23035 Sondalo (SO)
ITALIA
O
Vantive Manufacturing Limited
Moneen Road,
Castlebar, County Mayo, F23 XR63
Irlanda
Pueden solicitar más información respecto a este medicamento dirigiéndose al representante local del titular de la autorización de comercialización:
Vantive Health, S.L.
Polígono Industrial Sector 14.
C/ Pouet de Camilo, 2
46394 Ribarroja del Turia (Valencia)
España
Este medicamento está autorizado en los estados miembros del Espacio Económico
Europeoy en el Reino Unido (Irlanda del Norte)con los siguientes nombres:
Alemania, Austria, Bélgica, Bulgaria, Chipre, Dinamarca, Eslovaquia, Eslovenia, España,
Estonia, Finlandia, Francia, Grecia, Islandia, Irlanda, Italia, Letonia, Lituania, Luxemburgo,
Malta, Noruega, Países Bajos, Polonia, Portugal, Reino Unido (Irlanda del Norte), Rumanía y Suecia: Phoxilium
Hungría: Phoxil
Fecha de la última revisión de este prospecto:
10/2018
La información detallada y actualizada de este medicamento está disponible en la página Web de la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS) http://www.aemps.es
--------------------------------------------------------------------------------------------------------------------
Esta información está destinada únicamente a profesionales del sector sanitario
Phoxilium 1,2 mmol/l de fosfato
Solución para hemodiálisis y hemofiltración
Precauciones
Debe seguir con exactitud las instrucciones de uso y manipulaciónde Phoxilium.
Las soluciones de los dos compartimentos debenmezclarse antes de usarse.
El uso de una solución contaminada puede causar sepsis y shock.
Para aumentar la comodidad del paciente, se puede calentar Phoxilium hasta alcanzar los 37°C. El calentamiento previo al uso de la solución se debe realizar antes de la reconstitución utilizando solo calor seco. Las soluciones no se deben calentar en agua ni en un horno microondas. Antes de la administración, se debe comprobar visualmente que Phoxilium no contenga partículas ni haya perdido el color original. No administre la solución a menos que ésta sea transparente y el precinto esté intacto.
La concentración de fosfato inorgánico debe determinarse periódicamente. El fosfato inorgánico debe sustituirse en aquellos casos en los que el nivel de fosfato en sangre sea bajo.
La adición de bicarbonato sódico de sustitución puede aumentar el riesgo de alcalosis metabólica.
En caso de desequilibrio de líquidos, se debe supervisar minuciosamente la situación clínica y restaurar el equilibro de líquidos:
- En caso de hipervolemia, la velocidad de ultrafiltración neta prescrita para el dispositivo TCRR puede aumentarse y/o la velocidad de administración de aquellas soluciones distintas de los líquidos de rehidratación y/o el líquido de diálisis puede reducirse.
- En caso de hipovolemia, la velocidad de la ultrafiltración neta prescrita para el dispositivo de TCRR puede reducirse y/o la velocidad de administración de aquellas soluciones distintas de los líquidos de rehidratación y/o el líquido de diálisis puede aumentarse.
Advertencias:
Phoxilium no se debe utilizar en pacientes con hiperpotasemia. Se debe supervisar la concentración de potasio en el suero antes y durante la hemofiltración y/o la hemodiálisis.
Phoxilium es una solución que contiene potasio, por lo que puede provocar hiperpotasemia transitoria una vez iniciado el tratamiento. En tal caso, reduzca la velocidad de perfusión y asegúrese de que se haya alcanzado la concentración de potasio necesaria. Si la hiperpotasemia no remite, suspenda el tratamiento de inmediato.
Si se produce hiperpotasemia cuando se usa Phoxilium como líquido de diálisis, puede ser necesario administrar un líquido de diálisis sin potasio para aumentar la velocidad de eliminación del potasio.
Debido a que Phoxilium es una solución que contiene fosfato, puede provocar hiperfosfatemia temporal una vez iniciado el tratamiento. En tal caso, se debe reducir la velocidad de perfusión hasta alcanzar la concentración de fosfato deseada. Si la hiperfosfatemia no remite, la administración debe suspenderse de inmediato.
Los electrolitos y los parámetros ácido-básicos en sangre deben controlarse periódicamente en los pacientes tratados con Phoxilium. Phoxilium contiene hidrógeno fosfato, un ácido débil que puede afectar al equilibrio acidobásico del paciente. Si durante el tratamiento con Phoxilium aparece acidosis metabólica o esta empeora, es posible que sea necesario reducir la velocidad de perfusión o suspender la administración.
Phoxilium no contiene glucosa, por lo que su administración puede provocar hipoglucemia. Los niveles de glucosa en la sangre se deben supervisar con regularidad en los pacientes diabéticos (incluida una consideración minuciosa en el caso de los pacientes que tomen insulina u otros medicamentos hipoglucemiantes), pero también se deben tener en cuenta en los pacientes no diabéticos, debido, por ejemplo, al riesgo de hipoglucemia asintomática durante el procedimiento. Si se produce una hipoglucemia, se debe considerar el uso de una solución con glucosa. Pueden ser necesarias otras medidas correctoras para mantener el control glucémico deseado.
Posología:
El volumen y la velocidad a la que se administra Phoxilium dependen de la concentración de fosfato y otros electrolitos en la sangre, del equilibrio ácido-básico, del equilibrio de líquidos y del estado clínico general del paciente. El volumen de la solución de sustitución y/o del líquido de diálisis que se debe administrar también dependerá de la intensidad (dosis) del tratamiento deseada. La pauta de administración (dosis, velocidad de la perfusión y volumen acumulado) de Phoxilium solo debe determinarla un médico con experiencia en medicina intensiva y TCRR (terapia continua de reemplazo renal).
Por tanto, el volumen de la dosis lo determinará y prescribirá el médico responsable.
La velocidad de flujo de la solución de sustitución en terapias de hemofiltración y hemodiafiltración es:
Adultos: 500-3.000 ml/h
La velocidad de flujo del líquido de diálisis en terapias de hemodiálisis y hemodiafiltración continua es:
Adultos: 500-2.500 ml/h
La velocidad de flujo total combinada utilizada habitualmente para la TCRR (líquido de diálisis y soluciones de sustitución) en adultos es de 2.000 a 2.500 ml/h aproximadamente, lo que corresponde a un volumen de líquido diario aproximado de entre 48 y 60 l.
Población pediátrica:
En el caso de los niños, desde neonatos hasta adolescentes de hasta 18 años, el intervalo de velocidad de flujo cuando se utiliza como solución de sustitución en hemofiltración y hemodiafiltración y como solución de diálisis (líquido de diálisis) en hemodiálisis continua y hemodiafiltración continua es de 1.000 a 4.000 ml/h/1,73 m2.
En los adolescentes (de 12 a 18 años), cuando se calcule que la dosis pediátrica supera la dosis máxima para adultos, se debe utilizar la dosis recomendada para adultos.
Instrucciones de uso y manipulación
La solución del compartimento pequeño A se añade a la solución del compartimento grande B tras romper el vástago rompible e inmediatamente antes utilizarse. La solución reconstituida debe ser transparente e incolora.
Se debe emplear una técnica aséptica durante la manipulación y administración al paciente.
Utilizar solamente si el envoltorio está íntegro, los precintos están intactos, el vástago rompible no está roto y la solución es transparente. Apriete la bolsa firmemente para asegurarse de que no haya fugas. Si se descubre alguna fuga, deseche la solución inmediatamente ya que no se puede garantizar su esterilidad.
El compartimento grande B tiene un acceso de inyección para añadir otros fármacos que sean
necesarios una vez reconstituida la solución. Es responsabilidad del médico juzgar la compatibilidad de la medicación añadida a la solución Phoxilium comprobando el cambio eventual de color y/o precipitación, complejos insolubles o cristales. Antes de añadir un medicamento, verifique si es soluble y estable en este medicamento y que el rango de pH de Phoxilium es adecuado (el rango de pH de la solución reconstituida es 7,0-8,5). Los aditivos podrían no ser compatibles. Se deben consultar las instrucciones de uso del medicamento que se va a añadir.
Retire cualquier líquido del acceso de inyección, sujete la bolsa en posición vertical hacia abajo,
añada el fármaco a través del acceso de inyección y mezcle completamente. El mezclado de los aditivos siempre debe realizarse antes de conectar la bolsa de la solución al circuito estracorpóreo. La solución debe administrarse inmediatamente.
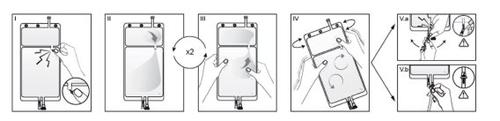
IRetire el envoltorio de la bolsa inmediatamente antes de usarla y deseche los demás materiales de embalaje. Abra el cierre rompiendo el vástago situado entre los dos compartimentos de la bolsa. El vástago permanece en la bolsa (vea la figura I que aparece abajo).
II.Asegúrese de que todo el líquido del compartimento pequeño A pase al compartimento grande B (vea la figura II que aparece abajo).
IIIAclare dos veces el compartimento pequeño A forzando la solución mezclada de vuelta a este compartimento pequeño A y luego otra vez al compartimento grande B (vea la figura III que aparece abajo).
IVUna vez vaciado el compartimento pequeño A, agite el compartimento grande B para que se mezcle completamente su contenido. La solución ya está lista para su uso y la bolsa puede colgarse en el equipo (vea la figura IV que aparece abajo).
VLa línea de líquido de diálisis o de sustitución puede conectarse a cualquiera de los dos conectores de acceso.
V.aSi se utiliza el acceso luer, retire el tapón utilizando una técnica aséptica y conecte el conector luer macho de la línea de líquido de diálisis o sustitución en el receptor luer hembra de la bolsa; hágalo fuertemente. Con ambas manos, rompa el vástago rompible de color azul por la base y muévalo adelante y atrás. No utilice herramientas. Compruebe que el vástago rompible está completamente separado y que el líquido circula libremente. El vástago rompible permanecerá en el puerto luer durante el tratamiento (vea la figura V.a que aparece abajo)
V.bSi se utiliza el acceso de inyección, retire primero el tapón levantándolo. El puerto de inyección es un puerto que se puede desinfectar con torunda. Introduzca después el espigón a través de la pared de goma. Compruebe que el líquido circula libremente (vea la figura V.b que aparece abajo)
La solución reconstituida debe utilizarse inmediatamente. En caso de no utilizarla inmediatamente, tenga en cuenta que la solución reconstituida debe utilizarse en el plazo de las 24 horas posteriores a la adición de la solución A a la solución B, incluida la duración del tratamiento.
La solución reconstituida es para un solo uso. Deseche la solución sobrante inmediatamente después del uso.
La eliminación del medicamento no utilizado y de todos los materiales que hayan estado en contacto con él, se realizará de acuerdo con la normativa local.
PHOXILIUM ES PVC CONECTOR LUER CON VÁLVULA; 2016-07
Composición de Phoxilium
A continuación se enumeran los principios activos antes y después de la mezcla (reconstitución)
de la solución.
Los principios activos antes de la mezcla son:
1.000 ml de solución del compartimento pequeño (A)contienen:
Cloruro de calcio, 2 H2O 3,68 g
Cloruro de magnesio, 6 H2O 2,44 g
1.000 ml de solución del compartimento grande (B)contienen:
Cloruro de sodio 6,44 g
Bicarbonato de sodio 2,92 g
Cloruro de potasio 0,314 g
Fosfato disódico, 2 H2O 0,225 g
Los principios activos después de la mezcla son:
Las soluciones de los compartimentos A (250 ml) y B (4.750 ml) se mezclan para producir una solución reconstituida (5.000 ml) cuya composición es la siguiente:
mmol/l
Calcio, Ca2+ 1,25
Magnesio, Mg2+ 0,6
Sodio, Na+ 140
Cloruro, Cl- 115,9
Hidrógenoosfato, HPO42- 1,2
Bicarbonato, HCO3- 30
Potasio, K+ 4
Osmolaridad teórica: 293 mOsm/l
Los demás componentes son:
Dióxido de carbono (para ajuste de pH) E290
Ácido clorhídrico (para ajuste de pH) E507
Agua para preparaciones inyectables
Aspecto del producto y contenido del envase
Phoxilium es una solución para hemodiálisis y hemofiltración que se presenta en una bolsa que consta de dos compartimentos. La solución final reconstituida se obtiene tras romper el vástago rompible y mezclar ambas soluciones. La solución reconstituida es transparente e incolora. Cada bolsa (A+B) contiene 5.000 ml de solución para hemodiálisis y hemofiltración. La bolsa está envuelta en película transparente.
Cada caja contiene dos bolsas y un prospecto.
Titular de la autorización de comercialización y responsable de la fabricación:
Vantive Belgium SRL
Boulevard d´Angleterre 2
1420 Braine-l´Alleud
Bélgica
Fabricante:
Bieffe Medital S.p.A
Via Stelvio 94,
23035 Sondalo (SO)
ITALIA
O
Vantive Manufacturing Limited
Moneen Road,
Castlebar, County Mayo, F23 XR63
Irlanda
Pueden solicitar más información respecto a este medicamento dirigiéndose al representante local del titular de la autorización de comercialización:
Vantive Health, S.L.
Polígono Industrial Sector 14.
C/ Pouet de Camilo, 2
46394 Ribarroja del Turia (Valencia)
España
Este medicamento está autorizado en los estados miembros del Espacio Económico
Europeo y en el Reino Unido (Irlanda del Norte) con los siguientes nombres:
Alemania, Austria, Bélgica, Bulgaria, Chipre, Dinamarca, Eslovaquia, Eslovenia, España,
Estonia, Finlandia, Francia, Grecia, Islandia, Irlanda, Italia, Letonia, Lituania, Luxemburgo,
Malta, Noruega, Países Bajos, Polonia, Portugal, Reino Unido (Irlanda del Norte), Rumanía y Suecia: Phoxilium
Hungría: Phoxil
Fecha de la última revisión de este prospecto:
10/2018
La información detallada y actualizada de este medicamento está disponible en la página Web de la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS) http://www.aemps.es
--------------------------------------------------------------------------------------------------------------------
Esta información está destinada únicamente a profesionales del sector sanitario
Phoxilium®1,2 mmol/l de fosfato
Solución para hemodiálisis y hemofiltración
Precauciones
Debe seguir con exactitud las instrucciones de uso y manipulaciónde Phoxilium.
Las soluciones de los compartimentos debenmezclarse antes de usarse.
El uso de una solución contaminada puede causar sepsis y shock.
Para aumentar la comodidad del paciente, se puede calentar Phoxilium hasta alcanzar los 37°C. El calentamiento previo al uso de la solución se debe realizar antes de la reconstitución utilizando solo calor seco. Las soluciones no se deben calentar en agua ni en un horno microondas. Antes de la administración, se debe comprobar visualmente que Phoxilium no contenga partículas ni haya perdido el color original. No administre la solución a menos que ésta sea transparente y el precinto esté intacto.
La concentración de fosfato inorgánico debe determinarse periódicamente. El fosfato inorgánico debe sustituirse en aquellos casos en los que el nivel de fosfato en sangre sea bajo.
La adición de bicarbonato de sodio de sustitución puede aumentar el riesgo de alcalosis metabólica.
En caso de desequilibrio de líquidos, se debe supervisar minuciosamente la situación clínica y restaurar el equilibro de líquidos:
- En caso de hipervolemia, la velocidad de ultrafiltración neta prescrita para el dispositivo de TCRR puede aumentarse y/o la velocidad de administración de aquellas soluciones distintas de los líquidos de rehidratación y/o el líquido de diálisis puede reducirse.
- En caso de hipovolemia, la velocidad de la ultrafiltración neta prescrita para el dispositivo de TCRR puede reducirse y/o la velocidad de administración de aquellas soluciones distintas de los líquidos de rehidratación y/o el líquido de diálisis puede aumentarse.
Advertencias:
Phoxilium no se debe utilizar en pacientes con hiperpotasemia. Se debe supervisar la concentración de potasio en el suero antes y durante la hemofiltración y/o la hemodiálisis.
Phoxilium es una solución que contiene potasio, por lo que puede provocar hiperpotasemia transitoria una vez iniciado el tratamiento. En tal caso, reduzca la velocidad de perfusión y asegúrese de que se haya alcanzado la concentración de potasio necesaria. Si la hiperpotasemia no remite, suspenda el tratamiento de inmediato.
Si se produce hiperpotasemia cuando se usa Phoxilium como líquido de diálisis, puede ser necesario administrar un líquido de diálisis sin potasio para aumentar la velocidad de eliminación del potasio.
Debido a que Phoxilium es una solución que contiene fosfato, puede provocar hiperfosfatemia temporal una vez iniciado el tratamiento. En tal caso, se debe reducir la velocidad de perfusión hasta alcanzar la concentración de fosfato deseada. Si la hiperfosfatemia no remite, la administración debe suspenderse de inmediato.
Los electrolitos y los parámetros ácido-básicos en sangre deben controlarse periódicamente en los pacientes tratados con Phoxilium. Phoxilium contiene hidrógenofosfato, un ácido débil que puede afectar al equilibrio acidobásico del paciente. Si durante el tratamiento con Phoxilium aparece acidosis metabólica o esta empeora, es posible que sea necesario reducir la velocidad de perfusión o suspender la administración.
Phoxilium no contiene glucosa, por lo que su administración puede provocar hipoglucemia. Los niveles de glucosa en la sangre se deben supervisar con regularidad en los pacientes diabéticos (incluida una consideración minuciosa en el caso de los pacientes que tomen insulina u otros medicamentos hipoglucemiantes), pero también se deben tener en cuenta en los pacientes no diabéticos, debido, por ejemplo, al riesgo de hipoglucemia asintomática durante el procedimiento. Si se produce una hipoglucemia, se debe considerar el uso de una solución con glucosa. Pueden ser necesarias otras medidas correctoras para mantener el control glucémico deseado.
Posología:
El volumen y la velocidad a la que se administra Phoxilium dependen de la concentración de fosfato y otros electrolitos en la sangre, del equilibrio ácido-básico, del equilibrio de líquidos y del estado clínico general del paciente. El volumen de la solución de sustitución y/o del líquido de diálisis que se debe administrar también dependerá de la intensidad (dosis) del tratamiento deseada. La pauta de administración (dosis, velocidad de la perfusión y volumen acumulado) de Phoxilium solo debe determinarla un médico con experiencia en medicina intensiva y TCRR (terapia continua de reemplazo renal).
Por tanto, el volumen de la dosis lo determinará y prescribirá el médico responsable.
La velocidad de flujo de la solución de sustitución en terapias de hemofiltración y
hemodiafiltración es:
Adultos: 500-3.000 ml/h
La velocidad de flujo de la solución de diálisis (líquido de diálisis) en terapias de hemodiálisis y hemodiafiltración continua es:
Adultos: 500-2.500 ml/h
La velocidad de flujo total combinada utilizada habitualmente para la TCRR (líquido de diálisis y soluciones de sustitución) en adultos es de 2.000 a 2.500 ml/h aproximadamente, lo que corresponde a un volumen de líquido diario aproximado de entre 48 y 60 l.
Población pediátrica:
En el caso de los niños, desde neonatos hasta adolescentes de hasta 18 años, el intervalo de velocidad de flujo cuando se utiliza como solución de sustitución en hemofiltración y hemodiafiltración y como solución de diálisis (líquido de diálisis) en hemodiálisis continua y hemodiafiltración continua es de 1.000 a 4.000 ml/h/1,73 m2.
En los adolescentes (de 12 a 18 años), cuando se calcule que la dosis pediátrica supera la dosis máxima para adultos, se debe utilizar la dosis recomendada para adultos.
Instrucciones de uso y manipulación
La solución del compartimento pequeño A se añade a la solución del compartimento grande B tras romper el vástago rompible e inmediatamente antes utilizarse. La solución reconstituida debe ser transparente e incolora.
Se debe emplear una técnica aséptica durante todo el proceso de administración al paciente.
Utilizar solamente si el envoltorio está íntegro, los precintos
están intactos, el vástago rompible no está roto y la solución es transparente. Apriete la bolsa firmemente para asegurarse de que no haya fugas. Si se descubre alguna fuga, deseche la solución inmediatamente ya que no
se puede garantizar su esterilidad.
El compartimento grande B tiene un acceso de inyección para añadir otros fármacos que sean necesarios una vez reconstituida la solución.Es responsabilidad del médico juzgar la compatibilidad de la medicación añadida a la solución Phoxilium comprobando el cambio eventual de color y/o precipitación, complejos insolubles o cristales. Antes de añadir un medicamento, verifique si es soluble y estable en este medicamento y que el rango de pH de Phoxilium es adecuado (el rango de pH de la solución reconstituida es 7,0-8,5). Los aditivos podrían no ser compatibles. Se deben consultar las instrucciones de uso del medicamento que se va a añadir.
Retire cualquier líquido del acceso de inyección, sujete la bolsa en posición vertical hacia abajo, añada el fármaco a través del acceso de inyección y mezcle completamente. El mezclado de los aditivos siempre debe realizarse antes de conectar la bolsa de la solución al circuito estracorpóreo. La solución debe administrarse inmediatamente.
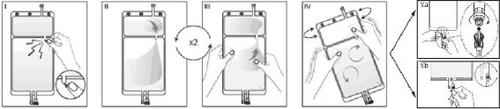
IRetire el envoltorio de la bolsa inmediatamente antes de usarla y deseche los demás materiales
de embalaje. Abra el cierre rompiendo el vástago situado entre los dos compartimentos de
la bolsa. El vástago permanece en la bolsa (vea la figura I que aparece abajo).
II.Asegúrese de que todo el líquido del compartimento pequeño A pase al compartimento
grande B (vea la figura II que aparece abajo).
IIIAclare dos veces el compartimento pequeño A forzando la solución mezclada de vuelta a este compartimento pequeño A y luego otra vez al compartimento grande B (vea la figura III que aparece abajo).
IVUna vez vaciado el compartimento pequeño A, agite el compartimento grande B para que se
mezcle completamente su contenido. La solución ya está lista para su uso y la bolsa puede
colgarse en el equipo (vea la figura IV que aparece abajo).
VLa línea de diálisis o de sustitución puede conectarse a cualquiera de los dos conectores de
acceso.
V.aSi se utiliza el acceso luer, quite el tapón con un movimiento de giro y extracción y conecte el conector luer macho de la línea de diálisis o sustitución en el receptor luer hembra de la bolsa mediante un movimiento de
empuje y giro. Asegúrese de que la conexión está bien hecha y apretada. La conexión se
abrirá. Compruebe que el líquido circula libremente (vea la figura V.a que aparece abajo).
Si la línea de diálisis o sustitución se desconecta del conector luer, el conector se cerrará y
el flujo de la solución se detendrá. El puerto luer es un puerto sin aguja que se puede
limpiar.
V.bSi se utiliza el acceso de inyección, retire primero el tapón levantándolo. El puerto de inyección es un puerto que se puede desinfectar con torunda. Introduzca después el espigón a través de la pared de goma. Compruebe que el líquido circula libremente (vea la figura V.b que aparece abajo).
La solución reconstituida debe utilizarse inmediatamente. En caso de no utilizarla inmediatamente, tenga en cuenta que la solución reconstituida debe utilizarse en el plazo de las 24 horas posteriores a la adición de la solución A a la solución B, incluida la duración del tratamiento.
La solución reconstituida es para un solo uso. Deseche la solución sobrante inmediatamente después del uso.
La eliminación del medicamento no utilizado y de todos los materiales que hayan estado en contacto con él, se realizará de acuerdo con la normativa local.
- País de registo
- Forma farmacêuticaHEMOFILTRAÇÃO, 1,2 mmol/L Fosfato
- Código ATCB05ZB91
- Substância ativa
- Requer receita médicaSim
- Fabricante
- Esta informação é apenas para fins informativos e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento.
- Alternativas a PHOXILIUM 1,2 mmol/L SOLUÇÃO DE FOSFATO PARA HEMODIÁLISE/HEMOFILTRAÇÃOForma farmacêutica: HEMOFILTRAÇÃO, 2 mmol potássio/lSubstância ativa: HemofiltratesFabricante: Nikkiso BelgiumRequer receita médicaForma farmacêutica: HEMOFILTRAÇÃO, 4 mmol potássio/lSubstância ativa: HemofiltratesFabricante: Nikkiso BelgiumRequer receita médicaForma farmacêutica: HEMOFILTRAÇÃO, -Substância ativa: HemofiltratesFabricante: Nikkiso BelgiumRequer receita médica
Médicos online para PHOXILIUM 1,2 mmol/L SOLUÇÃO DE FOSFATO PARA HEMODIÁLISE/HEMOFILTRAÇÃO
Avaliação de dosagem, efeitos secundários, interações, contraindicações e renovação de receita para PHOXILIUM 1,2 mmol/L SOLUÇÃO DE FOSFATO PARA HEMODIÁLISE/HEMOFILTRAÇÃO — sujeita a avaliação médica e à regulamentação local.
Obtenha uma receita de PHOXILIUM 1,2 mmol/L SOLUÇÃO DE FOSFATO PARA HEMODIÁLISE/HEMOFILTRAÇÃO online
Preencha um formulário de 2 minutos
Conte-nos os seus sintomas, historial e o medicamento que está a solicitar.
Escolha um médico ou deixe-nos atribuir
Escolha um especialista ou ligamos com o próximo médico disponível.
O médico analisa o seu caso
Normalmente em 30 minutos. Pode fazer perguntas adicionais por chat.
Levante em qualquer farmácia
Receita eletrónica enviada para o seu e-mail — válida em toda a Espanha.
Perguntas frequentes

Receba atualizações e ofertas exclusivas
Seja o primeiro a conhecer novos serviços, atualizações do marketplace e ofertas exclusivas para subscritores.