VEJICUR PÓ E SOLVENTE PARA SUSPENSÃO INTRAVESICAL

Como utilizar VEJICUR PÓ E SOLVENTE PARA SUSPENSÃO INTRAVESICAL
Traduzido com IA
Esta informação é fornecida apenas para fins informativos e não substitui a consulta de um médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
Mostrar originalConteúdo do folheto informativo
Introdução
Prospecto: informação para o utilizador
Vejicur pó e dissolvente para suspensão intravesical
Bacilo de Calmette-Guérin
Leia todo o prospecto atentamente antes de começar a usar este medicamento,pois contém informações importantes para si.
- Conserva este prospecto, pois pode ter que voltar a lê-lo.
- Se tiver alguma dúvida, consulte o seu médico ou farmacêutico.
- Se experimentar efeitos adversos, consulte o seu médico ou farmacêutico, mesmo que se trate de efeitos adversos que não aparecem neste prospecto. Ver secção 4.
Conteúdo do prospecto
- O que é Vejicur e para que é utilizado
- O que precisa saber antes de começar a usar Vejicur
- Como usar Vejicur
- Posíveis efeitos adversos
- Conservação de Vejicur
- Conteúdo do envase e informação adicional
1. O que é Vejicur e para que é utilizado
O nome completo deste medicamento é Vejicur pó e dissolvente para suspensão intravesical. Far-se-á referência ao mesmo como Vejicur no resto deste prospecto.
Vejicur contém bactérias da espécie Mycobacterium bovisdebilitadas (atenuadas) com um potencial infeccioso baixo.
Vejicur estimula o sistema imunitário e é utilizado para o tratamento de vários tipos de cancro na bexiga urinária. É eficaz se o cancro se limita às células que revestem o interior da bexiga (urotélio) e não invadiu os tecidos internos da bexiga.
Vejicur é administrado directamente na bexiga mediante instilação.
Para a forma de lesão plana de cancro de bexiga (carcinoma localizado), Vejicur é utilizado para curar a doença limitada ao revestimento da bexiga. Existem diferentes graus de cancro que afectam o revestimento da bexiga e as camadas de células próximas ao revestimento (lâmina própria).
Vejicur também é utilizado para prevenir a reaparição do cancro (tratamento profilático).
2. O que precisa saber antes de começar a usar Vejicur
Não use Vejicur
- se é alérgico à bactéria BCG (bacilo de Calmette-Guérin) viável ou a algum dos outros componentes deste medicamento (incluídos na secção 6)
- se há uma diminuição da actividade do seu sistema imunitário ou se sofre
imunodeficiências, tanto se se devem a uma doença simultânea (por exemplo, serologia positiva para VIH, leucemia, linfoma), ao tratamento do cancro (por exemplo, medicamentos citostáticos, radiação) ou a um tratamento imunossupressor (por exemplo, corticosteroides)
- se padece tuberculose activa
- se anteriormente recebeu radioterapia na bexiga ou regiões adjacentes
- se está em período de amamentação
- se lhe foi realizada uma intervenção cirúrgica através da uretra (RTU, ressecção transuretral), obteve uma amostra de tecido da sua bexiga (biopsia vesical) ou sofreu uma lesão por catéter (sondagem traumática) nas 2 ou 3 semanas anteriores.
- se tem perfuração na bexiga
- se a sua urina contém sangue visível (macrohematuria)
- se padece uma infecção aguda das vias urinárias.
Vejicur não deve ser utilizado para a administração subcutânea, intradérmica, intramuscular ou intravenosa, nem para vacinação. Deve ser administrado directamente na bexiga mediante instilação.
Advertências e precauções
O seu médico entrega-lhe uma carta de alerta para o doente, que deve sempre llevar consigo (ver também a secção 4).
Consulte o seu médico ou farmacêutico antes de começar a usar Vejicur
- se tem febre ou há presença de sangue na urina. Neste caso, o tratamento com Vejicur deve ser adiado
- se tem uma capacidade vesical baixa, pois pode diminuir ainda mais após o tratamento
- se é HLA-B27 (antígeno leucocitário humano B27) positivo, pois poderia apresentar um aumento da presença de inflamação das articulações (artrite reactiva)
- se tem artrite com inflamação da pele, dos olhos e das vias urinárias (síndrome de Reiter)
- se tem uma dilatação localizada de um vaso sanguíneo (aneurisma) ou prótese. Poderiam infectar-se os implantes ou enxertos.
- se tem problemas hepáticos ou toma medicamentos que podem afectar o fígado. Isto é de particular importância se se considera um tratamento antibiótico triplo com fármacos dos denominados antituberculosos.
Higiene geral
Após a instilação, sente-se para urinar, a fim de prevenir salpicaduras da urina e evitar a contaminação da área circundante com a bactéria BCG.
Recomenda-se lavar as mãos e os genitais após urinar. Isto é especialmente importante após urinar pela primeira vez após o tratamento com BCG. Se se contaminam lesões da pele, deve utilizar-se um desinfectante adequado (pergunte ao seu médico ou farmacêutico).
Detecção do bacilo de Calmette-Guérin
A detecção da bactéria BCG por lo geral é dificultosa. Um teste com resultado negativo não descarta uma infecção com BCG fora da bexiga.
Infecção das vias urinárias
O seu médico verificará que não padece uma infecção aguda das vias urinárias antes de cada tratamento vesical com BCG. Se for diagnosticada uma infecção aguda das vias urinárias durante o tratamento com BCG, deve interromper-se o tratamento até que os resultados da análise da urina sejam normais e termine o tratamento com antibióticos.
Pacientes em contacto com pessoas imunodeprimidas
Se recebe tratamento com Vejicur, deve atender às normas gerais de higiene enumeradas previamente. Isto é de máxima importância se está em contacto com pessoas imunodeprimidas, pois a bactéria BCG pode ser prejudicial para os doentes com um sistema imunitário debilitado. No entanto, até ao momento não se notificou nenhuma transmissão da bactéria de pessoa para pessoa.
Transmissão sexual
Deve usar preservativo nas relações sexuais durante a semana seguinte ao tratamento com BCG para assegurar que não se produz uma transmissão da bactéria BCG.
Outros medicamentos e Vejicur
Informa o seu médico ou farmacêutico se está a tomar, tomou recentemente ou poderia ter que tomar qualquer outro medicamento.
Isto é especialmente importante com os seguintes medicamentos, pois as bactérias BCG são sensíveis a:
- medicamentos antituberculosos (por exemplo, etambutol, estreptomicina, ácido p-aminosalicílico (PAS), isoniazida (INH) e rifampicina);
- antibióticos (fluoroquinolonas, doxiciclina ou gentamicina);
- antisépticos;
- lubrificantes.
As bactérias BCG são resistentes à pirazinamida e cicloserina.
Gravidez, amamentação e fertilidade
Gravidez
Não deve utilizar Vejicur se está grávida ou acredita que possa estar.
Amamentação
Vejicur está contraindicado durante a amamentação.
Fertilidade
Verificou-se que o BCG afecta negativamente a produção de espermatozoides e poderia causar uma concentração baixa ou a ausência de espermatozoides no sêmen. Este efeito foi reversível em animais. No entanto, os varões devem pedir conselho sobre a possibilidade de preservar espermatozoides antes de começar o tratamento.
Condução e uso de máquinas
Este medicamento pode afectar a capacidade para conduzir e utilizar máquinas. Não conduza nem utilize máquinas até que saiba que efeito tem Vejicur em si.
Consulte o seu médico, enfermeiro ou farmacêutico se tiver dúvidas.
3. Como usar Vejicur
Posologia
Será sempre um profissional de saúde com experiência quem preparará e lhe administrará Vejicur. É necessário o conteúdo de um frasco para um tratamento da bexiga.
Administração
Vejicur é introduzido na bexiga a baixa pressão mediante um catéter.
O medicamento deve permanecer na bexiga durante um período de 2 horas. Para isso, não deve beber durante um período de 4 horas antes do tratamento nem nas 2 horas seguintes ao tratamento.
Enquanto a suspensão permanece na bexiga, deve manter o contacto suficiente com toda a superfície mucosa; o mover-se de um lado para o outro ajuda ao tratamento. Após 2 horas, deve urinar, em posição sentada para evitar que salpique.
A menos que siga uma dieta baixa em líquidos, é aconselhável que beba abundantemente durante as 48 horas seguintes a cada tratamento.
Uso em crianças
Não foi estabelecida a segurança e eficácia do medicamento em crianças.
Uso em pessoas de idade avançada
Não há nenhuma instrução especial para o uso em pessoas de idade avançada. No entanto, deve considerar-se a função do fígado antes de administrar BCG.
Duração do tratamento
Como programa de tratamento padrão (tratamento de indução), receberá um tratamento intravesical com Vejicur à semana durante 6 semanas consecutivas. Após um período de 4 semanas sem tratamento, pode receber uma administração intravesical complementar, chamada tratamento de manutenção, durante pelo menos um ano tal como se descreve a seguir. O seu médico falará com si sobre isso.
Tratamento de indução
- O tratamento com BCG deve ser iniciado cerca de 2 – 3 semanas após a intervenção cirúrgica através da uretra (RTU, ressecção transuretral) ou da tomada de uma amostra de tecido vesical (biopsia vesical) e sem lesão por catéter (sondagem traumática). Deve ser repetido a intervalos semanais durante 6 semanas.
- Posteriormente, muitas pessoas recebem terapia de manutenção, durante a qual pode que se lhe administrem mais doses.
Tratamento de manutenção
- A terapia de manutenção consiste em 3 tratamentos a intervalos semanais administrados durante um mínimo de 1 ano até um máximo de 3 anos nos meses 3, 6, 12, 18, 24, 30 e 36. Com este programa, receberá um total de 15 a 27 tratamentos durante um período de um a três anos.
O seu médico analisará com si a necessidade de uma terapia de manutenção cada 6 meses após o primeiro ano de tratamento, se necessário.
Embora o tratamento de manutenção reduza a possibilidade de que o cancro reapareça e poderia reduzir a sua capacidade de progressão, os efeitos adversos e as molestias associados ao tratamento poderiam superar os benefícios em alguns doentes. Por isso, é importante que o seu médico comente com si as desvantagens do tratamento e as preferências que si tem antes de começar ou continuar o tratamento de manutenção.
Se usa mais Vejicur do que deve
É improvável que se produza uma sobredosagem, pois um frasco de Vejicur corresponde a uma dose que se instila na bexiga. Não há dados que indiquem que uma sobredosagem possa produzir qualquer outro sintoma distinto dos efeitos adversos descritos (ver secção 4).
4. Efeitos Adversos Possíveis
Tal como todos os medicamentos, este medicamento pode produzir efeitos adversos, embora nem todas as pessoas os sofram.
Os efeitos adversos do tratamento com BCG são frequentes, embora geralmente sejam leves e temporários. As reações adversas aumentam normalmente com o número de tratamentos de BCG.
No entanto, a reação adversa mais grave é uma infecção sistémica grave. Informe ao seu médico imediatamente se sofrer os seguintes sintomas, que podem aparecer a qualquer momento, e muitas vezes se diferem e podem aparecer semanas, meses ou mesmo anos após a última dose.
Mostre ao seu médico a sua carta de alerta para o paciente.
- Febre acima de 39,5 °C durante um mínimo de 12 horas ou febre de mais de 38 °C que dura semanas; suores noturnos
- Perda de peso de origem desconhecida
- Mal-estar crescente
- Os sinais de inflamação podem diferir, e apresentar-se como:
- dificuldades para respirar ou uma tos que não se percebem como um resfriado normal (pneumonia miliar),
- problemas hepáticos: sensação de pressão na parte superior direita do abdômen ou anomalias nas provas de função hepática (especialmente de uma enzima denominada fosfatase alcalina), ou
- dor e vermelhidão dos olhos, problemas de visão ou visão borrosa; conjuntivite
- Uma inflamação denominada granulomatosa que apareceu em uma biópsia.
Reação/infecção sistémica por BCG
Uma lesão acidental na bexiga durante o tratamento com BCG ou a administração de BCG em um músculo ou em uma veia podem dar origem a uma infecção generalizada grave por BCG. Uma infecção sistémica grave por BCG pode provocar sepsis por BCG. A sepsis por BCG é uma condição potencialmente mortal. Consulte imediatamente o seu médico se apresentar um sintoma ou sinal que o preocupe, ou contacte um médico especialista em doenças infecciosas. No entanto, a infecção não é virulenta. O seu médico lhe receitará medicamentos para as suas reações adversas, e pode ser que se interrompa o tratamento com BCG.
Em contraste com uma infecção por BCG, uma reação por BCG muitas vezes se apresenta com febrícula, sintomas pseudogripais e mal-estar geral durante 24 - 48 horas como início de uma reação imunológica. O seu médico lhe receitará algum medicamento para tratar os sintomas. Fale com o seu médico se os seus sintomas piorarem.
Infecção por BCG diferida
Em casos individuais, a bactéria BCG pode permanecer no organismo por anos. Esta infecção poderia apresentar-se a qualquer momento, e às vezes os sintomas e sinais de uma infecção se apresentam mais tarde, mesmo anos após a administração da última dose de BCG. Os sinais de inflamação poderiam ser semelhantes aos de uma infecção/reação grave ao BCG como se menciona previamente. Outros efeitos adversos do seu tratamento com BCG podem ser problemas em um implante ou enxerto, e requerem tratamento urgente.
Em consequência, é de máxima importância que leve a sua carta de alerta pessoal consigo e a entregue a cada médico que o trate, para assegurar o tratamento apropriado no caso de que apareça uma infecção por BCG diferida. O médico também poderá avaliar se os sintomas são uma reação adversa do seu tratamento com BCG ou não.
A seguir, uma lista completa de reações adversas que podem ocorrer:
Muito frequentes: podem afetar mais de 1 em cada 10 pessoas
- Náuseas (sentir-se mareado)
- Inflamação da bexiga (cistite), reações inflamatórias (granulomas) da bexiga. Estes efeitos adversos podem ser uma parte essencial da atividade antitumoral.
- Urinar com frequência com incômodo e dor; pode afetar até 90% dos pacientes.
- Reações inflamatórias da próstata (prostatite granulomatosa assintomática)
- Reações sistémicas e transitórias a BCG, tais como febre inferior a 38,5 °C, sintomas pseudogripais (mal-estar, febre, calafrios) e mal-estar geral
- Fadiga
Frequentes: podem afetar até 1 em cada 10 pessoas
- Febre superior a 38,5 °C
- Dor muscular (mialgia)
- Diarréia
- Dor abdominal
- Perda do controle da bexiga (incontinência urinária)
Pouco frequentes: podem afetar até 1 em cada 100 pessoas
- Reação/infecção sistémica e grave por BCG, septicemia por BCG (ver mais adiante a informação detalhada)
- Deficiência de células sanguíneas (citopenia)
- Anemia (diminuição da hemoglobina do sangue)
- Síndrome de Reiter (artrite com inflamação da pele, dos olhos e das vias urinárias)
- Inflamação dos pulmões (pneumonia miliar)
- Reações inflamatórias dos pulmões (granuloma pulmonar)
- Inflamação do fígado (hepatite)
- Abscesso cutâneo
- Erupção cutânea, inflamação das articulações (artrite), dor das articulações (artralgia). Na maioria dos casos, estes efeitos adversos são sinais de uma reação alérgica (hipersensibilidade) a BCG. Em alguns casos, pode ser necessário suspender o tratamento
- Infecção das vias urinárias, presença de sangue na urina (hematuria macroscópica)
- Bexiga de tamanho anormalmente pequeno (retração vesical), fluxo de urina anormalmente escasso (obstrução urinária), contractura vesical
- Inflamação dos testículos (orquite)
- Inflamação do epidídimo (epididimite)
- Reação inflamatória da próstata (prostatite granulomatosa sintomática)
- Tensão arterial baixa (hipotensão)
- Prova de função hepática anormal
Raros: podem afetar até 1 em cada 1.000 pessoas
- Infecção vascular (por exemplo: dilatação localizada infectada de um vaso sanguíneo)
- Abscesso renal
Muito raros: podem afetar até 1 em cada 10.000 pessoas
- Infecção por BCG dos implantes e tecidos circundantes (por exemplo: infecção do enxerto aórtico, desfibrilador cardíaco, artroplastia de quadril ou joelho)
- Inflamação dos gânglios linfáticos do pescoço (linfadenite cervical), infecção dos gânglios linfáticos regionais
- Reação alérgica (hipersensibilidade) (por exemplo: edema dos párpados, tos)
- Inflamação do interior do olho (coriorretinite)
- Conjuntivite (olhos vermelhos), uveíte (inflamação da úvea do olho)
- Fístula vascular
- Vômitos, fístula intestinal, inflamação do peritônio (peritonite)
- Infecção de ossos e da medula óssea por bactérias (osteomielite)
- Infecção da medula óssea
- Abscesso do psoas (abscesso no músculo da virilha)
- Inflamação dos testículos (orquite) ou epidídimo (epididimite) resistente ao tratamento antituberculoso
- Infecção do glande
- Inchaço nos braços e nas pernas
Frequência não conhecida: não pode ser estimada a partir dos dados disponíveis
- Inflamação dos vasos sanguíneos (pode ser no cérebro)
- Distúrbios dos genitais (por exemplo: dor de vagina)
- Relações sexuais dolorosas (dispareunia)
- Reação imunológica grave com febre, aumento do tamanho do fígado, do baço e dos gânglios linfáticos, icterícia e erupção cutânea (síndrome hemofagocítico)
- Insuficiência renal, inflamação do tecido renal, dos cálices e da pelve (pielonefrite, nefrite [incluindo nefrite tubulointersticial, nefrite intersticial e glomerulonefrite])
- Ausência ou nível baixo de espermatozoides no sêmen (azoospermia, oligozoospermia)
- Antígeno prostático específico elevado (PSA, um exame clínico da próstata)
Comunicação de efeitos adversos
Se experimentar qualquer tipo de efeito adverso, consulte o seu médico ou farmacêutico, mesmo que se trate de possíveis efeitos adversos que não aparecem neste prospecto. Também pode comunicá-los diretamente através do Sistema Espanhol de Farmacovigilância de Medicamentos de Uso Humano: www.notificaRAM.es. Mediante a comunicação de efeitos adversos, você pode contribuir para fornecer mais informações sobre a segurança deste medicamento.
5. Conservação de Vejicur
Mantenha este medicamento fora da vista e do alcance das crianças.
Não utilize este medicamento após a data de validade que aparece na etiqueta e na caixa após CAD.
Conservar na geladeira (entre 2 °C e 8 °C).
Não congelar.
Conservar no embalagem original para protegê-lo da luz.
Foi demonstrada a estabilidade em uso física e química durante 24 horas quando se conserva o medicamento protegido da luz a temperatura ambiente (entre 20 °C e 25 °C) ou a temperatura de geladeira (entre 2 °C e 8 °C).
Desde um ponto de vista microbiológico, o medicamento deve ser utilizado imediatamente.
Se não for utilizado imediatamente, os tempos e as condições de conservação em uso previos à sua utilização são responsabilidade do usuário e normalmente não excederão 24 horas entre 2 °C e 8 °C, a menos que a reconstituição tenha sido realizada em condições assépticas controladas e validadas.
6. Conteúdo do frasco e informações adicionais
Composição de Vejicur
O princípio ativo é a bactéria BCG (bacilo de Calmette-Guérin) viável (cepa RIVM derivada da cepa 1173-P2).
Após a reconstituição, um frasco contém:
Cepa RIVM da BCG derivada da cepa 1173-P2
2 x 10^8 a 3 x 10^9 unidades viáveis
Os outros componentes do pó são: poligelina, glicose anidra e polissorbato 80.
Os outros componentes do solvente são: cloreto de sódio e água para injetáveis.
Aspecto do produto e conteúdo do frasco
Vejicur é formado por um pó branco ou quase branco, ou uma massa porosa com tons amarelos e cinzas, e uma solução incolor e transparente usada como solvente. É apresentado em frascos de 1, 3, 5 ou 6 vias com ou sem cateter(es) e conector(es) Luer-Lock a cônico(s). Pode ser que apenas alguns tamanhos de frascos sejam comercializados.
Título da autorização de comercialização e responsável pela fabricação
medac
Gesellschaft für
klinische Spezialpräparate mbH
Theaterstr. 6
22880 Wedel
Alemanha
Podem solicitar mais informações sobre este medicamento dirigindo-se ao representante local do titular da autorização de comercialização:
Laboratórios Gebro Pharma, S.A.
Av. Tibidabo, 29
08022 Barcelona
Espanha
Data da última revisão desteprospecto: 03/2025
A informação detalhada e atualizada deste medicamento está disponível no site da Agência Espanhola de Medicamentos e Produtos Sanitários (AEMPS) http://www.aemps.gob.es/
-----------------------------------------------------------------------------------------------------------------------------
Esta informação está destinada apenas a profissionais do setor sanitário:
Tratamento de sintomas, de sinais e do síndrome
Sintomas, sinais ou síndrome | Tratamento |
| Tratamento sintomático |
| Interromper o tratamento com Vejicur e iniciar tratamento com quinolonas. Se após 10 dias não se observou a resolução completa, administrar isoniazida (INH)* durante 3 meses. Em caso de tratamento antituberculoso, o tratamento com Vejicur deve suspender-se definitivamente |
| Adiar o tratamento com Vejicur até que a análise de urina seja normal e tenha concluído o tratamento com antibióticos. |
| Interromper o tratamento com Vejicur. Considerar uma consulta com um especialista em doenças infecciosas. Administrar isoniazida (INH)* e rifampicina*, durante 3-6 meses segundo a gravidade. Em caso de tratamento antituberculoso, o tratamento com Vejicur deve suspender-se definitivamente |
| Tratamento sintomático com paracetamol |
| Suspender o tratamento com Vejicur. Considerar uma consulta com um especialista em doenças infecciosas. Administrar antihistamínicos ou anti-inflamatórios não esteroides. Deve-se considerar um tratamento com cortisona em caso de uma reação imunomediada. Se não houver resposta, administrar isoniazida* durante 3 meses. Em caso de tratamento antituberculoso, a terapia com Vejicur deve suspender-se definitivamente. |
| Suspender definitivamente o tratamento com Vejicur. Considerar consultar com um especialista em doenças infecciosas. Administrar tratamento antituberculoso com três fármacos * durante 6 meses, e tratamento com corticosteroides em doses baixas. |
| Suspender definitivamente o tratamento com Vejicur. Administrar imediatamente tratamento antituberculoso* com 3 fármacos combinado com corticoesteroides de ação rápida a altas doses. Consultar com um especialista em doenças infecciosas. |
- Precaução: As bactérias BCG são sensíveis a todos os medicamentos antituberculosos, atualmente utilizados, exceto a pirazinamida. Se for necessário um tratamento antituberculoso com 3 fármacos, a combinação geralmente recomendada é isoniazida (INH), rifampicina e etambutol.
** ver definição anterior
Informação importante sobre o uso de Vejicur
Vejicur só deve ser usado por profissionais sanitários com experiência.
Certifique-se de que a conservação é apropriada (ver seção 5) e confirme a integridade do frasco.
Vejicur deve ser administrado nas condições requeridas para endoscopia intravesical.
Vejicur não se deve administrar por via subcutânea, intradérmica, intramuscular ou intravenosa nem para vacinação contra a tuberculose.
O conector para catéter Luer-Lock da bolsa de solvente só se deve usar para instilação intravesical!
Princípios básicos e medidas de proteção para o uso de Vejicur
Em geral, deve-se evitar o contato direto com Vejicur. Vejicur é um medicamento que pode causar infecção nos seres humanos e representar um risco para os profissionais sanitários. Pode existir um risco se o medicamento entrar no organismo através de pele lesionada, se se inalarem aerossóis, se gotículas entrarem nos olhos ou entrarem em contato com as mucosas ou se se ingerir. Não coma, beba nem fume nas áreas de trabalho nem armazene alimentos, bebidas ou produtos de tabaco nelas. Vejicur não se deve manipular em uma sala em que se preparem medicamentos citotóxicos para uso por via intravenosa nem deve ser manipulado por pessoal que prepare medicamentos citotóxicos para uso por via intravenosa.
O medicamento não se deve manipular por pessoas com imunodeficiência conhecida.
Recomenda-se usar uma bata protetora fechada a prova de salpicaduras, luvas descartáveis, uma máscara respiratória FFP2 e óculos de segurança com protetores laterais como equipamento de proteção pessoal durante a manipulação. Vejicur só se deve transportar em recipientes fechados (para as condições de conservação após a reconstituição, ver seção 5).
Uma vez finalizado o trabalho, limpe as superfícies de trabalho com uma solução desinfetante adequada. Após o trabalho e em caso de contato com a pele, desinfete as mãos com um desinfetante para mãos, deixe-as secar, lave-as e use produtos para o cuidado da pele.
Testes cutâneos com tuberculina
O tratamento intravesical com Vejicur pode induzir sensibilidade à tuberculina e complicar a posterior interpretação do teste cutâneo da tuberculina para o diagnóstico de infecções micobacterianas. Portanto, deve-se medir a reatividade à tuberculina antes da administração de Vejicur.
Preparação da suspensão intravesical reconstituída
Antes do uso, o medicamento se deve ressuspender em condições assépticas com uma solução estéril de cloreto de sódio a 0,9 % (9 mg/ml) (ver as instruções de uso, passo 7). O catéter se deve colocar com especial cuidado para evitar lesões no epitélio da uretra e na bexiga urinária, que podem causar uma infecção sistêmica pelo BCG. Recomenda-se usar um lubrificante para reduzir ao mínimo o risco de um sondagem traumático e para tornar mais confortável o procedimento. As mulheres podem precisar de menos lubrificante do que os homens. Não se observou que um possível efeito antiséptico do lubrificante possa influir na eficácia do medicamento. Esvazie a bexiga após o sondagem para reduzir a quantidade de lubrificante que possa ter sido introduzida antes de administrar Vejicur. A suspensão se mistura removendo-a suavemente antes do uso. As partículas visíveis macroscopicamente não influem na eficácia e segurança do medicamento.
O conteúdo do frasco está previsto apenas para um único uso/uma única dose. Se deve descartar a suspensão restante.
A eliminação do medicamento não utilizado e de todos os materiais que tenham estado em contato com ele se realizará de acordo com a normativa local.
Conduta em caso de emergências e derramamento de Vejicur
Use roupa de proteção e evite remover o pó.
Cubra a suspensão de Vejicur derramada com celulosa e umedecê-la com um desinfetante com eficácia demonstrada contra as micobactérias. Após limpar a suspensão de Vejicur derramada, limpe novamente a superfície com uma solução desinfetante e deixe que seque. Os derramamentos sobre a pele se devem tratar com um desinfetante adequado.
Primeiros socorros
Consultar sempre um médico em caso de contaminação.
Em caso de contato com a pele: retirar a roupa contaminada. Desinfetar e limpar a pele e verificar se há contaminação de feridas.
Em caso de contato com os olhos: enxaguar o olho afetado com uma quantidade suficiente de solução de colírio ou, de forma alternativa, com água. Retirar as lentes de contato, se for o caso.
Em caso de ingestão: enxaguar a boca com água abundante.
Em caso de inalação: assegurar um suprimento suficiente de ar fresco.
Para mais informações sobre o catéter, consulte as instruções de uso correspondentes.
Instruções para os usuários de Vejicur
Componentes e aplicação do kit de instilação|
Componentes principais do kit de instilação
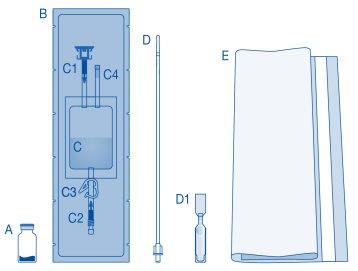
Componente principal | Descrição |
A | Frasco com pó |
B | Funda protetora |
C | Bolsa de solvente com solução de cloreto de sódio a 0,9 % (9 mg/ml) |
C1 | Conector para frasco com tampa protetora e selo de ruptura |
C2 | Conector para catéter Luer-Lock com tampa protetora e selo de ruptura |
C3 | Pina de pressão |
C4 | Porto de enchimento sem função de aplicação |
D | Catéter Luer-Lock |
D1 | Lubrificante |
E | Bolsa para descartáveis |
Conexão do frasco à bolsa de solvente
- Prepare a bolsa para descartáveis (E) para a eliminação direta do kit após a instilação para evitar uma contaminação.
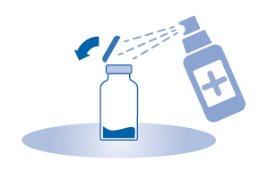
- Retire a cápsula de fechamento extraíble do frasco (A) e desinfete o tampão conforme a normativa local.
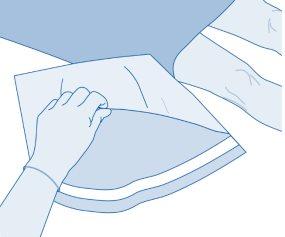
- Abra a funda protetora (B) da bolsa de solvente (C) e retire completamente a funda protetora.
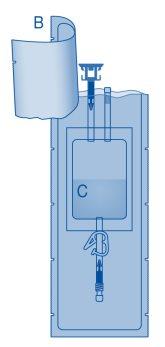
- Retire a tampa protetora do conector para frasco (C1).
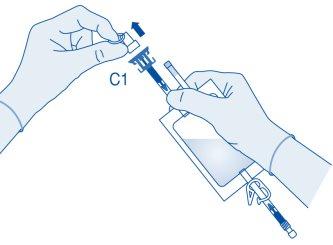
- Pressione o conector sobre o frasco até o topo.
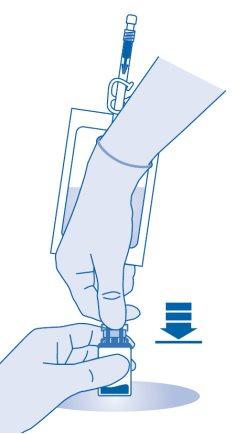
Mistura do pó com o solvente
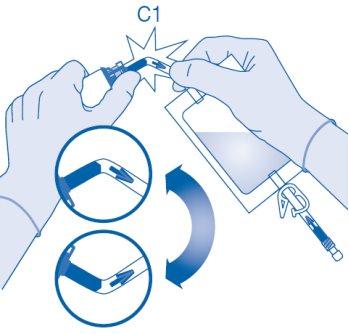
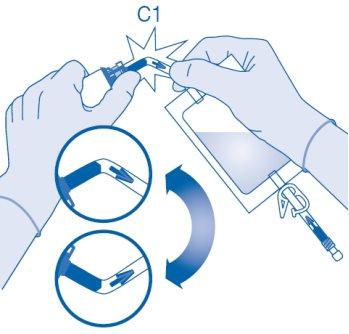
- Dobre o selo de ruptura dentro do tubo do conector para frasco (C1) para cima e para baixo várias vezes para romper o selo.
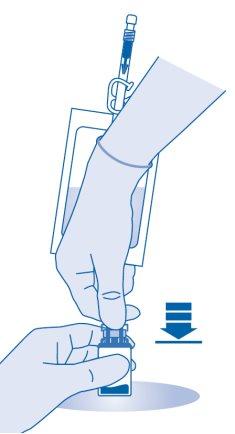
- Sostenha a bolsa de solvente de maneira que o frasco esteja abaixo dela.
Comprima a bolsa de solvente várias vezes para transferir quantidade suficiente de solvente para o frasco.
Certifique-se de nãoencher completamente o frasco para permitir a posterior transferência da suspensão para a bolsa de solvente. Pode restar certa quantidade de solvente no interior da bolsa.
Remova o frasco lentamentepara reduzir ao mínimo a formação abundante de espuma ao misturar o medicamento com o solvente. Se houver muita espuma, deixe o frasco repousar brevemente (vários minutos).
O conteúdo do frasco tem que formar uma suspensão homogênea. Isso pode levar vários minutos.
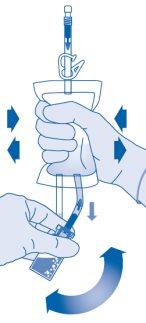
- Inverta a bolsa de solvente e sostenha-a de forma que o frasco esteja acima dela.
Sostenha o frasco.
Comprima a bolsa de solvente várias vezes até que o frasco esteja completamente vazio.
Se restar pó no interior do frasco, repita os passos 7 e 8.
Do ponto de vista microbiológico, o medicamento se deve usar imediatamente. Se o medicamento não se usar imediatamente, consulte a seção 5 “Conservação de Vejicur”.
A suspensão não se deve instilar a temperatura de geladeira para evitar que o paciente sinta a necessidade de urinar, o que acortaria o tempo de exposição.
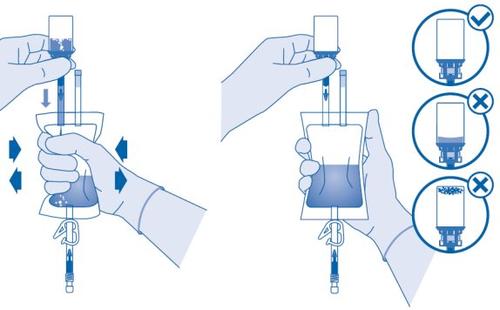
Sondagem
- Sonde o paciente conforme a normativa local e às instruções de uso utilizando o catéter Luer-Lock (D) e o lubrificante (D1) incluídos ou outro catéter e/ou lubrificante adequados.
Esvazie a bexiga urinária com o catéter.
Conexão do catéter à bolsa de solvente
- Para misturar os sedimentos que possam haver, gire e remova a bolsa antes de conectar.
Não administre a suspensão a temperatura de geladeira.
Retire a tampa protetora do conector para catéter (C2).
Conecte o catéter Luer-Lock do paciente (D) ao conector para catéter (C2) da bolsa de solvente.
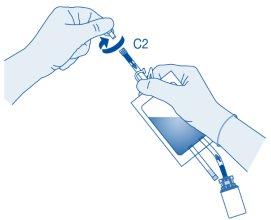
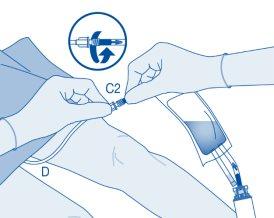
Instilação
- Dobre o selo de ruptura dentro do tubo do conector para catéter (C2) para cima e para baixo várias vezes para romper o selo.
Sostenha firmemente o catéter do paciente enquanto o faz.
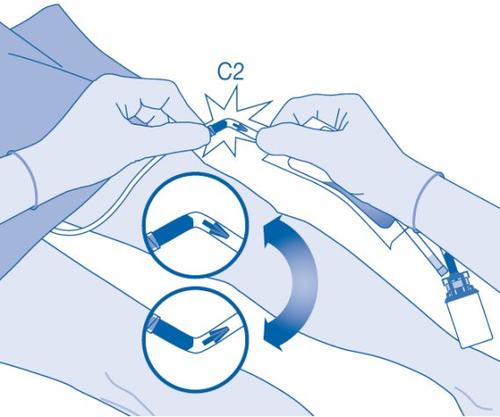
- Sostenha a bolsa de solvente com o frasco invertido por cima da bolsa.
Comprima a bolsa de solvente suavementecom a outra mão para instilar lentamenteo medicamento na bexiga urinária do paciente.
Continue comprimindo a bolsa de solvente até que esta e o frasco estejam vazios.
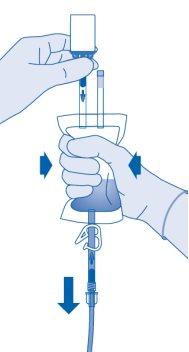
- Comprima a bolsa de solvente para expulsar o ar restante para esvaziar o catéter na maior medida possível.
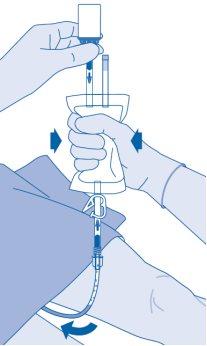
Após a instilação
- O fechamento da pina de pressão (C3) impede um refluxo de líquido ao catéter e reduz ao mínimo o risco de contaminação. De forma alternativa, pode manter comprimida a bolsa de solvente enquanto realiza os passos 15 e 16.
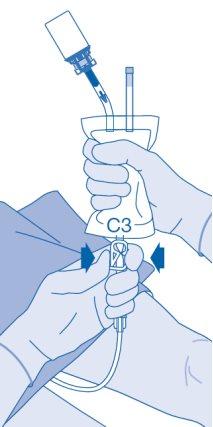
- Extraia com cuidado o catéter da bexiga sem desconectar a bolsa de solvente do catéter. Evite a contaminação por salpicadura de gotículas.
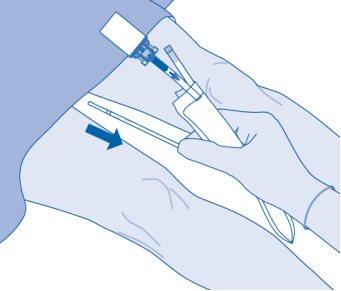
- Elimine o produto conforme os regulamentos nacionais utilizando a bolsa para descartáveis.
O conteúdo do frasco está previsto apenas para um único uso/uma única dose. Se deve descartar a suspensão restante.
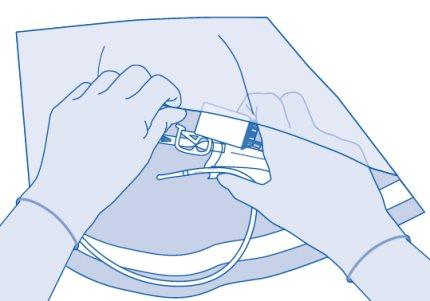
Instruções para os usuários de Vejicur
Componentes e aplicação do kit de instilação|
Componentes principais do kit de instilação
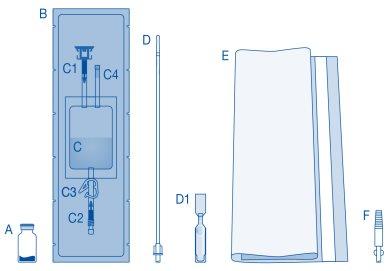
Componente principal | Descrição |
A | Frasco com pó |
B | Funda protetora |
C | Bolsa de solvente com solução de cloreto de sódio a 0,9 % (9 mg/ml) |
C1 | Conector para frasco com tampa protetora e selo de ruptura |
C2 | Conector para catéter Luer-Lock com tampa protetora e selo de ruptura |
C3 | Pina de pressão |
C4 | Porto de enchimento sem função de aplicação |
D | Catéter Luer-Lock |
D1 | Lubrificante |
E | Bolsa para descartáveis |
F | Conector Luer-Lock cónico |
Conexão do frasco à bolsa de dissolvente
- Prepare a bolsa para descartáveis (E) para a eliminação direta do kit após a instilação para evitar contaminação.
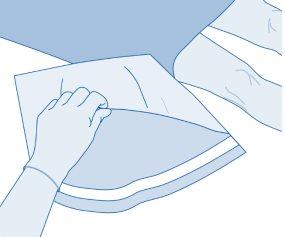
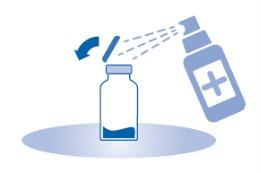
- Retire a cápsula de fechamento extraível do frasco (A) e desinfete o batoque conforme à normativa local.
- Abra a capa protetora (B) da bolsa de dissolvente (C) e retire completamente a capa protetora.
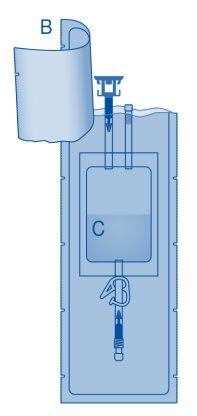
- Retire a tampa protetora do conector para frasco (C1).
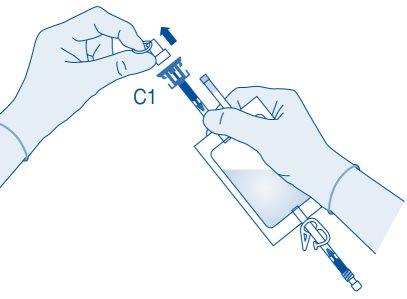
- Pressione o conector sobre o frasco até o topo.
Mistura do pó com o dissolvente
- Dobre o lacre de ruptura dentro do tubo do conector para frasco (C1) para cima e para baixo várias vezes para romper o lacre.
- Segure a bolsa de dissolvente de maneira que o frasco esteja abaixo dela.
Comprima a bolsa de dissolvente várias vezes para transferir quantidade suficiente de dissolvente para o frasco.
Certifique-se de nãoencher completamente o frasco para permitir a transferência posterior da suspensão para a bolsa de dissolvente. Pode restar certa quantidade de dissolvente no interior da bolsa.
Remova o frasco lentamentepara reduzir ao mínimo a formação abundante de espuma ao misturar o medicamento com o dissolvente. Se houver muita espuma, deixe o frasco repousar brevemente (vários minutos).
O conteúdo do frasco tem que formar uma suspensão homogênea. Isso pode levar vários minutos.
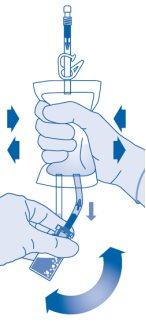
- Inverta a bolsa de dissolvente e segure-a de forma que o frasco esteja acima dela.
Segure o frasco.
Comprima a bolsa de dissolvente várias vezes até que o frasco esteja completamente vazio.
Se restar pó no interior do frasco, repita os passos 7 e 8.
Do ponto de vista microbiológico, o medicamento deve ser usado imediatamente.
Se o medicamento não for usado imediatamente, consulte a seção 5 “Conservação de Vejicur”.
A suspensão não deve ser instilada a temperatura de geladeira para evitar que o paciente sinta a necessidade de urinar, o que encurtaria o tempo de exposição.
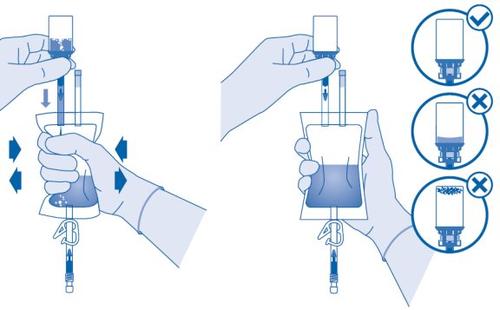
Sondagem
- Sonde o paciente conforme à normativa local e às instruções de uso utilizando um catéter e um lubrificante adequados.
Esvazie a bexiga urinária com o catéter.
Nota para o uso com um catéter auto-selecionado com conector cônico:
Deve-se usar o conector Luer-Lock cônico (F) incluído para conectar a bolsa ao catéter auto-selecionado (não mostrado).
Para isso, devem ser realizados os seguintes passos adicionais:
- Retire a tampa protetora do conector para catéter (C2, ver passo 10).
- Gire e remova a bolsa antes de conectá-la para re-misturar os sedimentos que possam haver.
- Conecte o conector Luer-Lock cônico (F) ao conector para catéter (C2) da bolsa.
- Conecte com cuidado a bolsa com o conector (F) ao catéter do paciente.
- Em seguida, continue no passo 11.
Conexão do catéter à bolsa de dissolvente
- Para misturar os sedimentos que possam haver, gire e remova a bolsa antes de conectá-la.
Não administre a suspensão a temperatura de geladeira.
Retire a tampa protetora do conector para catéter (C2).
Conecte o catéter Luer-Lock do paciente (D) ao conector para catéter (C2) da bolsa de dissolvente.
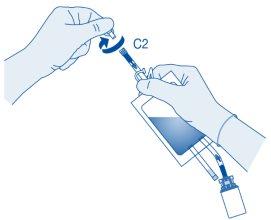
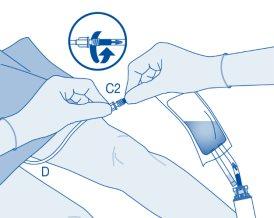
Instilação
- Dobre o lacre de ruptura dentro do tubo do conector para catéter (C2) para cima e para baixo várias vezes para romper o lacre.
Segure firmemente o catéter do paciente enquanto o faz.
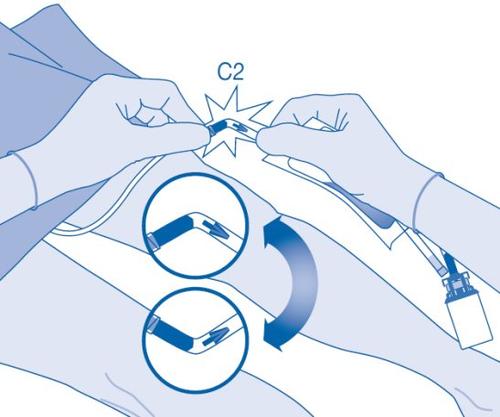
- Segure a bolsa de dissolvente com o frasco invertido acima da bolsa.
Comprima a bolsa de dissolvente suavementecom a outra mão para instilar lentamenteo medicamento na bexiga urinária do paciente.
Continue comprimindo a bolsa de dissolvente até que esta e o frasco estejam vazios.
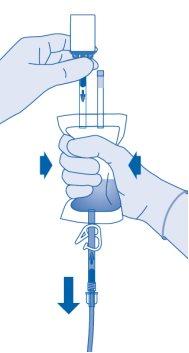
- Comprima a bolsa de dissolvente para expulsar o ar restante para esvaziar o catéter na maior medida possível.
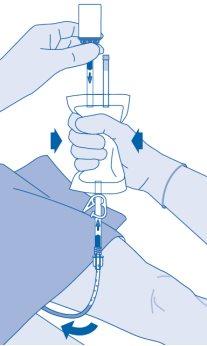
Após a instilação
- O fechamento da pinça de pressão (C3) impede um refluxo de líquido ao catéter e reduz ao mínimo o risco de contaminação. De forma alternativa, pode manter comprimida a bolsa de dissolvente enquanto realiza os passos 15 e 16.
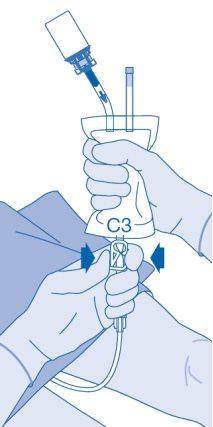
- Extraia com cuidado o catéter da bexiga sem desconectar a bolsa de dissolvente do catéter. Evite a contaminação por salpicadura de gotículas.
- Elimine o produto conforme os regulamentos nacionais utilizando a bolsa para descartáveis.
O conteúdo do frasco está previsto apenas para um único uso/uma única dose. Deve-se descartar a suspensão restante.
Instruções para os usuários de Vejicur
Componentes e aplicação do kit de instilação|
Componentes principais do kit de instilação
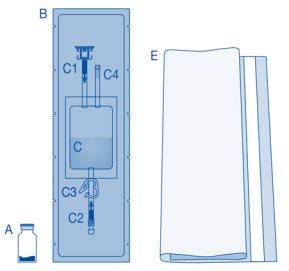
Componente principal | Descrição |
A | Frasco com pó |
B | Capa protetora |
C | Bolsa de dissolvente com solução de cloreto de sódio a 0,9% (9 mg/ml) |
C1 | Conector para frasco com tampa protetora e lacre de ruptura |
C2 | Conector para catéter Luer-Lock com tampa protetora e lacre de ruptura |
C3 | Pinça de pressão |
C4 | Porto de enchimento sem função de aplicação |
E | Bolsa para descartáveis |
Conexão do frasco à bolsa de dissolvente
- Prepare a bolsa para descartáveis (E) para a eliminação direta do kit após a instilação para evitar contaminação.
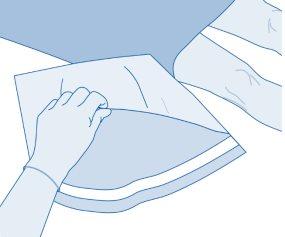
- Retire a cápsula de fechamento extraível do frasco (A) e desinfete o batoque conforme à normativa local.
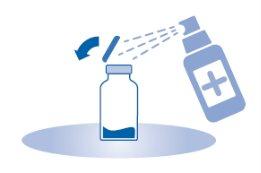
- Abra a capa protetora (B) da bolsa de dissolvente (C) e retire completamente a capa protetora.
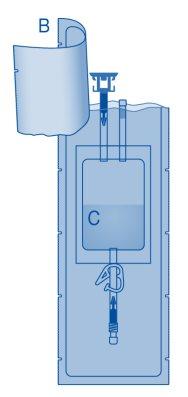
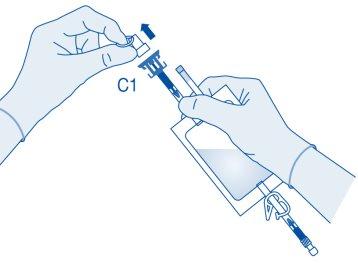
- Retire a tampa protetora do conector para frasco (C1).
- Pressione o conector sobre o frasco até o topo.
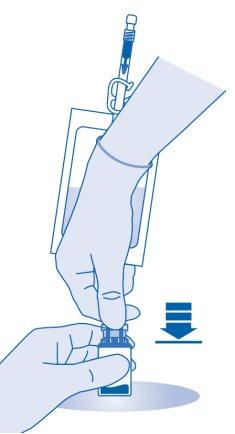
Mistura do pó com o dissolvente
- Dobre o lacre de ruptura dentro do tubo do conector para frasco (C1) para cima e para baixo várias vezes para romper o lacre.
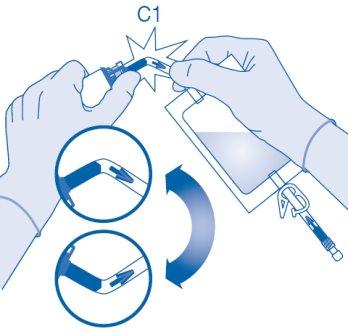
- Segure a bolsa de dissolvente de maneira que o frasco esteja abaixo dela.
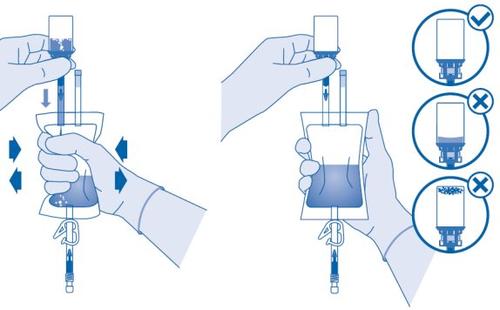
Comprima a bolsa de dissolvente várias vezes para transferir quantidade suficiente de dissolvente para o frasco.
Certifique-se de nãoencher completamente o frasco para permitir a transferência posterior da suspensão para a bolsa de dissolvente. Pode restar certa quantidade de dissolvente no interior da bolsa.
Remova o frasco lentamentepara reduzir ao mínimo a formação abundante de espuma ao misturar o medicamento com o dissolvente. Se houver muita espuma, deixe o frasco repousar brevemente (vários minutos).
O conteúdo do frasco tem que formar uma suspensão homogênea. Isso pode levar vários minutos.
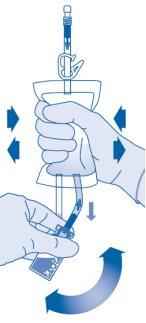
- Inverta a bolsa de dissolvente e segure-a de forma que o frasco esteja acima dela.
Segure o frasco.
Comprima a bolsa de dissolvente várias vezes até que o frasco esteja completamente vazio.
Se restar pó no interior do frasco, repita os passos 7 e 8.
Do ponto de vista microbiológico, o medicamento deve ser usado imediatamente.
Se o medicamento não for usado imediatamente, consulte a seção 5 “Conservação de Vejicur”.
A suspensão não deve ser instilada a temperatura de geladeira para evitar que o paciente sinta a necessidade de urinar, o que encurtaria o tempo de exposição.
Sondagem
- Sonde o paciente conforme à normativa local e às instruções de uso utilizando um catéter e um lubrificante adequados.
Esvazie a bexiga urinária com o catéter.
Conexão do catéter à bolsa de dissolvente
- Para misturar os sedimentos que possam haver, gire e remova a bolsa antes de conectá-la.
Não administre a suspensão a temperatura de geladeira.
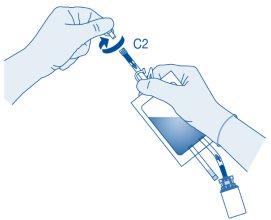
Retire a tampa protetora do conector para catéter (C2).
Conecte o catéter do paciente ao conector para catéter (C2) da bolsa de dissolvente.
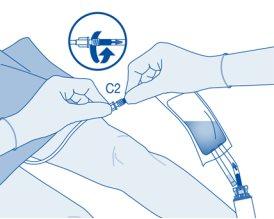
Instilação
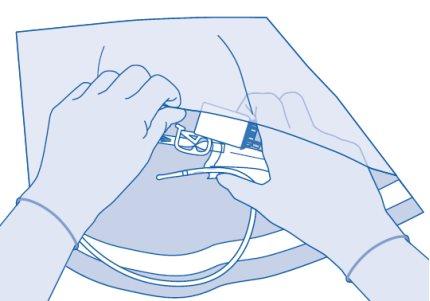
- Dobre o lacre de ruptura dentro do tubo do conector para catéter (C2) para cima e para baixo várias vezes para romper o lacre.
Segure firmemente o catéter do paciente enquanto o faz.
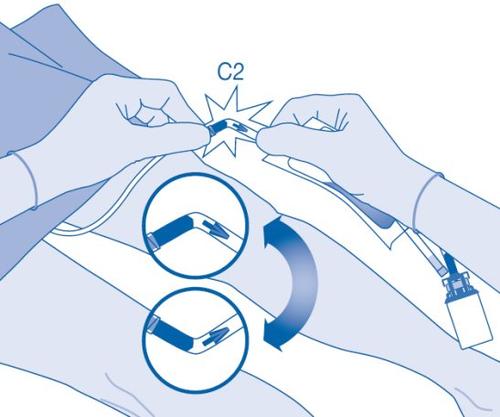
- Segure a bolsa de dissolvente com o frasco invertido acima da bolsa.
Comprima a bolsa de dissolvente suavementecom a outra mão para instilar lentamenteo medicamento na bexiga urinária do paciente.
Continue comprimindo a bolsa de dissolvente até que esta e o frasco estejam vazios.
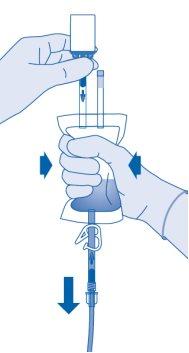
- Comprima a bolsa de dissolvente para expulsar o ar restante para esvaziar o catéter na maior medida possível.
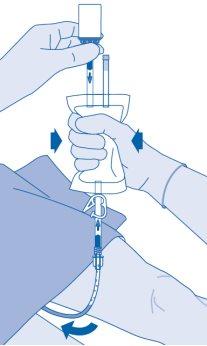
Após a instilação
- O fechamento da pinça de pressão (C3) impede um refluxo de líquido ao catéter e reduz ao mínimo o risco de contaminação. De forma alternativa, pode manter comprimida a bolsa de dissolvente enquanto realiza os passos 15 e 16.
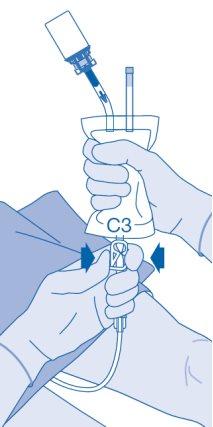
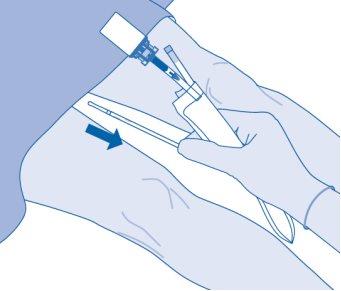
- Extraia com cuidado o catéter da bexiga sem desconectar a bolsa de dissolvente do catéter. Evite a contaminação por salpicadura de gotículas.
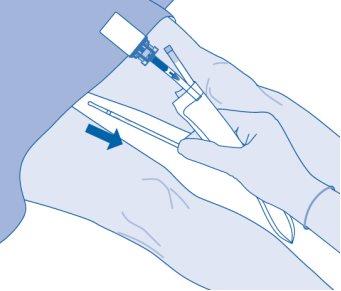
- Elimine o produto conforme os regulamentos nacionais utilizando a bolsa para descartáveis.
O conteúdo do frasco está previsto apenas para um único uso/uma única dose. Deve-se descartar a suspensão restante.
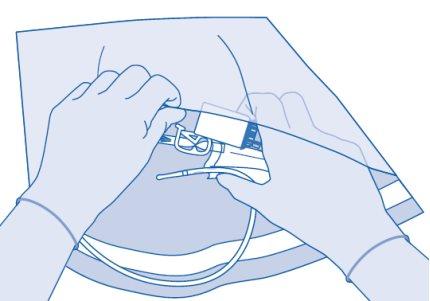
Instruções para os usuários de Vejicur
Componentes e aplicação do kit de instilação|
Componentes principais do kit de instilação
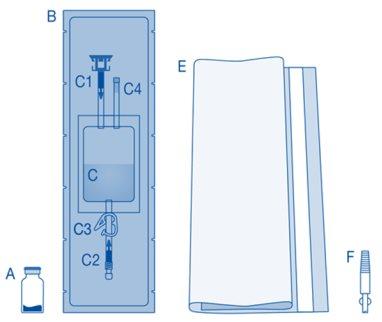
Componente principal | Descrição |
A | Frasco com pó |
B | Capa protetora |
C | Bolsa de dissolvente com solução de cloreto de sódio a 0,9% (9 mg/ml) |
C1 | Conector para frasco com tampa protetora e lacre de ruptura |
C2 | Conector para catéter Luer-Lock com tampa protetora e lacre de ruptura |
C3 | Pinça de pressão |
C4 | Porto de enchimento sem função de aplicação |
E | Bolsa para descartáveis |
F | Conector Luer-Lock cônico |
Conexão do frasco à bolsa de dissolvente
- Prepare a bolsa para descartáveis (E) para a eliminação direta do kit após a instilação para evitar contaminação.
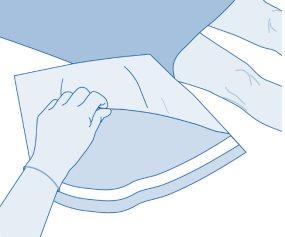
- Retire a cápsula de fechamento extraível do frasco (A) e desinfete o batoque conforme à normativa local.
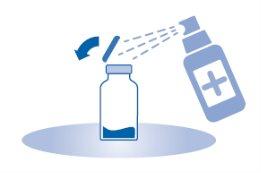
- Abra a capa protetora (B) da bolsa de dissolvente (C) e retire completamente a capa protetora.
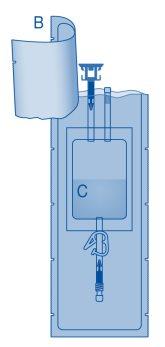
- Retire a tampa protetora do conector para frasco (C1).
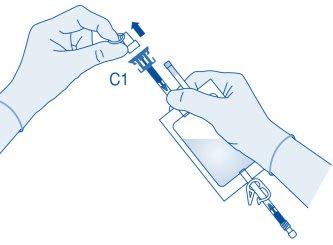
- Pressione o conector sobre o frasco até o topo.
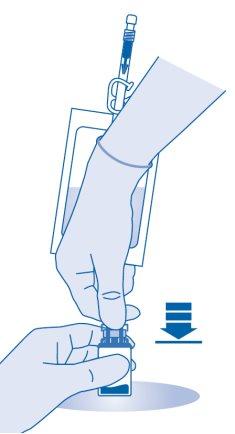
Mistura do pó com o dissolvente
- Dobre o lacre de ruptura dentro do tubo do conector para frasco (C1) para cima e para baixo várias vezes para romper o lacre.
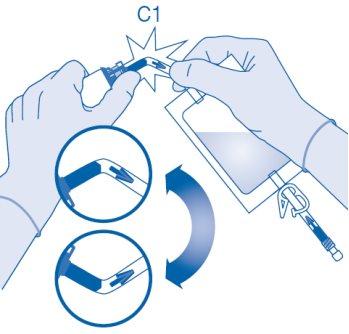
- Segure a bolsa de dissolvente de maneira que o frasco esteja abaixo dela.
Comprima a bolsa de dissolvente várias vezes para transferir quantidade suficiente de dissolvente para o frasco.
Certifique-se de nãoencher completamente o frasco para permitir a transferência posterior da suspensão para a bolsa de dissolvente. Pode restar certa quantidade de dissolvente no interior da bolsa.
Remova o frasco lentamentepara reduzir ao mínimo a formação abundante de espuma ao misturar o medicamento com o dissolvente. Se houver muita espuma, deixe o frasco repousar brevemente (vários minutos).
O conteúdo do frasco tem que formar uma suspensão homogênea. Isso pode levar vários minutos.
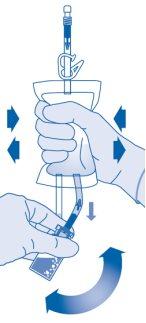
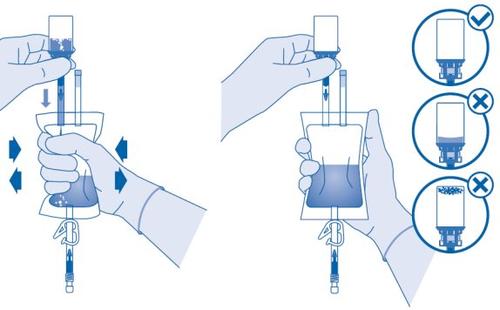
- Inverta a bolsa de dissolvente e segure-a de forma que o frasco esteja acima dela.
Segure o frasco.
Comprima a bolsa de dissolvente várias vezes até que o frasco esteja completamente vazio.
Se restar pó no interior do frasco, repita os passos 7 e 8.
Do ponto de vista microbiológico, o medicamento deve ser usado imediatamente.
Se o medicamento não for usado imediatamente, consulte a seção 5 “Conservação de Vejicur”.
A suspensão não deve ser instilada a temperatura de geladeira para evitar que o paciente sinta a necessidade de urinar, o que encurtaria o tempo de exposição.
A suspensão não deve ser instilada a temperatura de frigorífico, a fim de evitar que o paciente sinta a necessidade de urinar, o que encurtaria o tempo de exposição.
Sondagem
- Sonde o paciente de acordo com a normativa local e as instruções de uso, utilizando um cateter e um lubrificante adequados.
Esvazie a bexiga urinária com o cateter.
Este recipiente não contém um cateter. Utilize o conector (F) incluído para conectar a bolsa ao cateter do paciente com um conector cônico (não mostrado).
Para isso, devem ser realizadas as seguintes etapas adicionais:
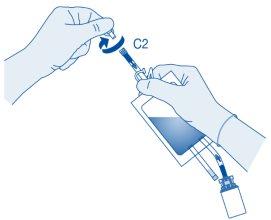
- Retire a tampa protetora do conector para cateter (C2, ver passo 10).
- Conecte o conector (F) ao conector para cateter (C2) da bolsa.
- Conecte com cuidado a bolsa com o conector (F) ao cateter do paciente.
- Em seguida, continue no passo 11.
Conexão do cateter à bolsa de dissolvente
- Para misturar os sedimentos que possam existir, gire e remova a bolsa antes de conectá-la.
Não administre a suspensão a temperatura de frigorífico.
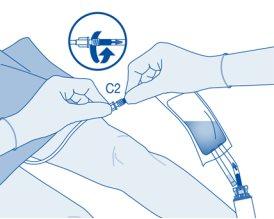
Retire a tampa protetora do conector para cateter (C2).
Conecte o cateter do paciente ao conector para cateter (C2) da bolsa de dissolvente.
Instilação
- Dobre o lacre de ruptura dentro do tubo do conector para cateter (C2) para cima e para baixo várias vezes para romper o lacre.
Segure firmemente o cateter do paciente enquanto o faz.
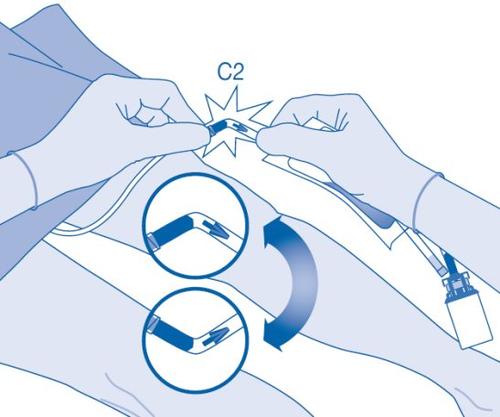
- Segure a bolsa de dissolvente com o frasco invertido acima da bolsa.
Comprima a bolsa de dissolvente suavementecom a outra mão para instilar lentamenteo medicamento na bexiga urinária do paciente.
Continue comprimindo a bolsa de dissolvente até que esta e o frasco estejam vazios.
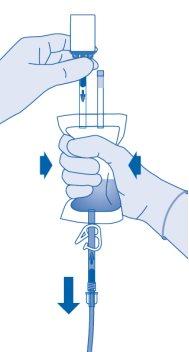
- Comprima a bolsa de dissolvente para expulsar o ar restante e esvaziar o cateter na maior medida possível.
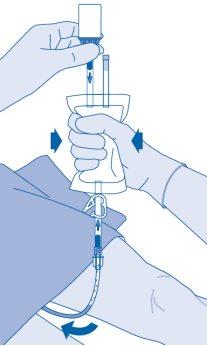
Após a instilação
- O fechamento da pinça de pressão (C3) impede um refluxo de líquido ao cateter e reduz ao mínimo o risco de contaminação. Alternativamente, pode manter comprimida a bolsa de dissolvente enquanto realiza os passos 15 e 16.
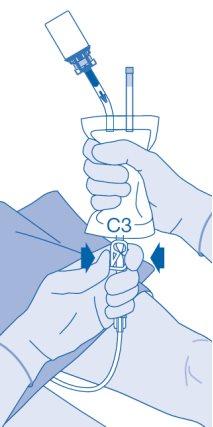
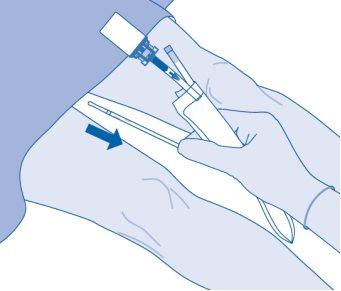
- Retire com cuidado o cateter da bexiga sem desconectar a bolsa de dissolvente do cateter. Evite a contaminação por salpicadura de gotículas.
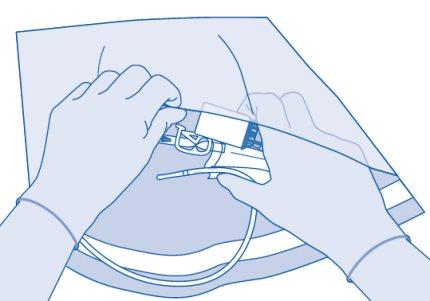
- Elimine o produto de acordo com os regulamentos nacionais, utilizando a bolsa para descartáveis.
O conteúdo do frasco é previsto apenas para um único uso/uma única dose. Deve-se descartar a suspensão restante.
- País de registo
- Forma farmacêuticaSOLUÇÃO PARA IRRIGAÇÃO VESICAL, 2 Unidades
- Código ATCL03AX03
- Substância ativa
- Requer receita médicaSim
- Fabricante
- Esta informação é apenas para fins informativos e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento.
- Alternativas a VEJICUR PÓ E SOLVENTE PARA SUSPENSÃO INTRAVESICALForma farmacêutica: SOLUÇÃO PARA IRRIGAÇÃO VESICAL, BCG (CULTURA VIVA LIOFILIZADA) 2-8 x 10(8) UFCSubstância ativa: BCG vaccineFabricante: Merck Sharp & Dohme De Espana S.A.Requer receita médicaForma farmacêutica: INJETÁVEL, DesconhecidaSubstância ativa: tasonerminFabricante: Belpharma S.A.Requer receita médicaForma farmacêutica: INJETÁVEL, 0,5 mg de cloridrato de histamina/0,5 mLSubstância ativa: histamine dihydrochlorideFabricante: Laboratoires DelbertRequer receita médica
Médicos online para VEJICUR PÓ E SOLVENTE PARA SUSPENSÃO INTRAVESICAL
Avaliação de dosagem, efeitos secundários, interações, contraindicações e renovação de receita para VEJICUR PÓ E SOLVENTE PARA SUSPENSÃO INTRAVESICAL — sujeita a avaliação médica e à regulamentação local.
Perguntas frequentes

Receba atualizações e ofertas exclusivas
Seja o primeiro a conhecer novos serviços, atualizações do marketplace e ofertas exclusivas para subscritores.