ILARIS 150 mg PÓ PARA SOLUÇÃO INJETÁVEL

Como utilizar ILARIS 150 mg PÓ PARA SOLUÇÃO INJETÁVEL
Traduzido com IA
Esta informação é fornecida apenas para fins informativos e não substitui a consulta de um médico. Consulte sempre um médico antes de tomar qualquer medicamento. A Oladoctor não se responsabiliza por decisões médicas baseadas neste conteúdo.
Mostrar originalConteúdo do folheto informativo
Introdução
Prospecto: informação para o utilizador
Ilaris 150mg/ml solução injectável
canakinumab
Leia todo o prospecto atentamente antes de começar a usar este medicamento, porque contém informações importantes para si.
- Conserva este prospecto, porque pode ter que voltar a lê-lo.
- Se tiver alguma dúvida, consulte o seu médico, farmacêutico ou enfermeiro.
- Este medicamento foi-lhe prescrito apenas para si, e não deve dá-lo a outras pessoas, mesmo que tenham os mesmos sintomas que si, porque pode prejudicá-las.
- Se experimentar efeitos adversos, consulte o seu médico, farmacêutico ou enfermeiro, mesmo que se trate de efeitos adversos que não aparecem neste prospecto. Ver secção 4.
Além deste prospecto, será entregue um cartão para o doente, que contém informações de segurança importantes que necessita antes e durante o tratamento com Ilaris.
Conteúdo do prospecto
- O que é Ilaris e para que é utilizado
- O que necessita saber antes de começar a usar Ilaris
- Como usar Ilaris
- Posíveis efeitos adversos
- Conservação de Ilaris
- Conteúdo do envase e informações adicionais
1. O que é Ilaris e para que é utilizado
O que é Ilaris
Ilaris contém o princípio ativo canakinumab, um anticorpo monoclonal que pertence ao grupo de medicamentos denominados inibidores de interleucinas. No organismo bloqueia a atividade de uma substância chamada interleucina-1 beta (IL-1 beta), que se encontra a níveis elevados nas doenças inflamatórias.
Para que é utilizado Ilaris
Ilaris é utilizado para o tratamento das seguintes doenças inflamatórias:
- Síndromes de febre periódica:
- síndromes periódicos associados à criopirina (CAPS*)
- síndrome periódico associado ao receptor do factor de necrose tumoral (TRAPS*)
- síndrome de hiperimunoglobulina D (HIDS*)/deficiência de mevalonato quinase (MKD*)
- febre mediterrânea familiar (FMF).
- Doença de Still, incluindo a doença de Still do adulto (ESA) e a artrite idiopática juvenil sistémica (AIJS)
- Gota artrítica
(*) por suas siglas em inglês
A seguir, inclui-se mais informação sobre estas doenças.
Síndromes de febre periódica
Ilaris é utilizado em adultos e crianças a partir de 2 anos para tratar as seguintes doenças:
- Síndromes periódicos associados à criopirina (CAPS) – é um grupo de doenças autoinflamatórias, que inclui:
- síndrome de Muckle-Wells (MWS)
- doença neonatal multisistémica inflamatória (NOMID), também conhecida como síndrome infantil neurológico, cutâneo e articular crónico (CINCA)
- manifestações graves do síndrome autoinflamatório familiar induzido pelo frio (FCAS) / urticária familiar fria (FCU) que apresente sinais e sintomas além da erupção cutânea de tipo urticária induzida pelo frio.
- Síndrome periódico associado ao receptor do factor de necrose tumoral (TRAPS)
- Síndrome de hiperimunoglobulina D (HIDS)/deficiência de mevalonato quinase (MKD)
- Febre Mediterrânea familiar (FMF): Ilaris é utilizado para tratar a FMF. Ilaris pode ser utilizado juntamente com colchicina, se for apropriado.
Em doentes com síndromes de febre periódica (CAPS, TRAPS, HIDS/MKD e FMF), o organismo produz demasiada IL-1 beta. Isto pode causar febre, dor de cabeça, fadiga, erupção cutânea ou dores nas articulações e músculos. Mediante o bloqueio da atividade de IL-1 beta, Ilaris pode melhorar estes sintomas.
Doença de Still
Ilaris é utilizado em doentes adultos, adolescentes e crianças a partir dos 2 anos de idade para o tratamento da doença de Still ativa, incluindo a doença de Still do adulto (ESA) e a artrite idiopática juvenil sistémica (AIJS) quando os outros tratamentos não tenham funcionado bem. Ilaris pode ser utilizado sozinho ou em combinação com metotrexato.
A doença de Still, que inclui AIJS e ESA, é uma doença inflamatória que pode provocar dor, inchaço e inflamação de uma ou mais articulações, bem como sarpilho e febre. A proteína pro-inflamatória IL-1beta desempenha um papel importante na inflamação da doença de Still. Ilaris pode melhorar os sinais e sintomas da doença de Still bloqueando a atividade de IL-1beta.
Gota artrítica
Ilaris é utilizado em adultos para tratar os sintomas de ataques frequentes de gota artrítica se outros tratamentos não tenham funcionado suficientemente bem.
A gota artrítica é causada pela formação de cristais de urato. Estes cristais de urato causam uma produção excessiva de IL-1 beta, que por sua vez pode provocar um dolor grave súbito, vermelhidão, calor e inchaço das articulações (conhecido como ataque de gota). Mediante o bloqueio de IL-1 beta, Ilaris pode conseguir melhorar estes sintomas.
2. O que necessita saber antes de começar a usar Ilaris
Não use Ilaris
- se é alérgico ao canakinumab ou a algum dos outros componentes deste medicamento (incluídos na secção 6)
- se tem, ou suspeita que tem, uma infecção grave e ativa.
Advertências e precauções
Consulte o seu médico antes de começar a usar Ilaris, se se encontra em alguma das seguintes situações:
- se padece alguma infecção atualmente ou se teve infecções repetidas ou sofre alguma doença tal como nível baixo de glóbulos brancos que o torna mais vulnerável a ter infecções
- se tem ou já teve tuberculose ou contacto direto com uma pessoa com uma infecção ativa de tuberculose. O seu médico pode verificar se tem tuberculose utilizando um teste específico
- se tem sinais de um distúrbio do fígado, tais como coloração amarela da pele e dos olhos, náuseas, perda de apetite, cor escura na urina e fezes branqueadas
- se tem que receber alguma vacina. Recomenda-se evitar ser vacinado com um tipo de vacina (também conhecida como vacina atenuada) enquanto está a usar Ilaris (ver também «Uso de Ilaris com outros medicamentos»).
- Este medicamento contém 0,6 mg de polissorbato 80 em cada frasco. Os polissorbatos podem causar reações alérgicas. Informe o seu médico se si ou o seu filho têm alguma alergia conhecida.
Doença de Still
- Os doentes com doença de Still podem desenvolver uma doença chamada síndrome de ativação macrofágica (SAM) que pode causar a morte. O seu médico fará um acompanhamento dos possíveis fatores desencadeantes de SAM, que incluem infecções e reativação da doença de Still (piora).
Rastreabilidade
Cada vez que si/o seu filho receber um novo envase de Ilaris, é importante que anote o nome do medicamento e a data de administração, juntamente com o número do lote, e que conserve esta informação num local seguro.
Crianças e adolescentes
- CAPS, TRAPS, HIDS/MKD, FMF e AIJS:Ilaris pode ser utilizado em crianças a partir de 2 anos de idade.
- Gota artrítica:Ilaris não é recomendado para crianças ou adolescentes menores de 18 anos de idade.
Outros medicamentos e Ilaris
Informe o seu médico, farmacêutico ou enfermeiro se está a usar, usou recentemente ou pode ter que usar qualquer outro medicamento.
- Vacinas atenuadas: recomenda-se evitar ser vacinado com um tipo de vacina conhecida como vacina atenuada enquanto está em tratamento com Ilaris. Pode ser que o seu médico necessite verificar o seu histórico de vacinações e dar-lhe aquelas vacinas que não recebeu antes de iniciar o tratamento com Ilaris. Se for necessário que lhe administrem uma vacina atenuada após iniciar o tratamento com Ilaris, comente com o seu médico. Uma vacina atenuada deve ser administrada normalmente 3 meses após a última injeção de Ilaris e 3 meses antes da seguinte.
- Medicamentos conhecidos como os inibidores do factor de necrose tumoral (TNF), tais como etanercept, adalimumab ou infliximab. Estes são utilizados principalmente em doenças reumáticas e autoimunes. Não devem ser utilizados com Ilaris porque podem aumentar o risco de infecções.
Gravidez e amamentação
Se está grávida ou em período de amamentação, acredita que possa estar grávida ou tem intenção de engravidar, consulte o seu médico ou farmacêutico antes de usar este medicamento.
- Deve evitar engravidar e recomenda-se utilizar medidas anticonceptivas adequadas enquanto estiver a tomar Ilaris e durante pelo menos três meses após a última administração. É importante que informe o seu médico se está grávida, se pode estar grávida ou se está a planear ter um bebé. O seu médico informá-lo-á sobre o risco potencial de usar Ilaris durante a gravidez.
- Se receber canakinumab enquanto está grávida, é importante que informe o pediatra ou enfermeiro antes de que lhe administrem alguma vacina ao seu bebé. O seu bebé não deve receber vacinas vivas até pelo menos 16 semanas após a última dose de canakinumab que recebeu antes do parto.
- Desconhece-se se Ilaris passa para o leite materno. O seu médico informá-lo-á sobre os riscos potenciais de usar Ilaris antes de amamentar.
Condução e uso de máquinas
O tratamento com Ilaris pode produzir-lhe uma sensação de que tudo dá voltas (tontura ou vertigem) ou cansaço intenso (astenia). Isto deve ser tido em conta quando avaliar a sua capacidade para realizar tarefas que requerem julgamento ou habilidades motoras. Se notar a sensação de que tudo lhe dá voltas ou se sentir cansado, não conduza nem use ferramentas ou máquinas até que se sinta de novo bem.
3. Como usar Ilaris
Siga exactamente as instruções de administração deste medicamento indicadas pelo seu médico. Em caso de dúvida, consulte novamente o seu médico, farmacêutico ou enfermeiro.
Mantenha o seu médico informado sobre a sua doença e sobre qualquer sintoma antes de usar ou de lhe ser administrado Ilaris (ver secção 2). O seu médico pode decidir adiar ou interromper o seu tratamento, apenas quando for necessário.
Ilaris deve ser utilizado por via subcutânea. Isto significa que é injectado com uma agulha curta dentro do tecido adiposo por debaixo da pele.
Se tem gota artrítica, um médico com formação especializada supervisionará o seu tratamento. Ilaris só deve ser injectado por um profissional de saúde.
Se tem CAPS, TRAPS, HIDS/MKD, FMF ou doença de Still (ESA ou AIJS), pode injectar-se a si mesmo com Ilaris após receber uma formação adequada, ou pode ser injectado por um cuidador.
Quanto Ilaris deve usar
Síndromes periódicos associados à criopirina (CAPS)
A dose inicial recomendada de Ilaris é:
- Adultos e crianças de 4anos ou mais
- 150 mg para doentes que pesam mais de 40 kg
- 2 mg/kg para doentes que pesam entre 15 kg e 40 kg
- 4 mg/kg para doentes que pesam entre 7,5 kg e menos de 15 kg
- Crianças de2 ou 3anos
- 4 mg/kg para doentes cujo peso corporal seja de 7,5 kg ou mais
Ilaris é injectado cada 8 semanas como uma injeção única.
- Se não responder suficientemente ao tratamento aos 7 dias, o seu médico pode dar-lhe outra dose de 150 mg ou 2 mg/kg.
- Se responder suficientemente à segunda dose, o seu tratamento continuará com 300 mg ou 4 mg/kg cada 8 semanas.
- Se não responder suficientemente à segunda dose, pode ser administrada uma terceira dose de Ilaris a 300 mg ou 4 mg/kg.
- Se responder suficientemente à terceira dose, o seu tratamento continuará com 600 mg ou 8 mg/kg cada 8 semanas.
Em crianças que iniciaram com uma dose inicial de 4 mg/kg e que não responderam suficientemente após 7 dias, o médico pode dar-lhe uma segunda dose de 4 mg/kg. Se a criança responder suficientemente a esta, pode continuar o tratamento com uma dose de 8 mg/kg cada 8 semanas.
Síndrome periódico associado ao receptor do factor de necrose tumoral (TRAPS), síndrome de hiperimunoglobulina D (HIDS)/deficiência de mevalonato quinase (MKD) e febre Mediterrânea familiar (FMF)
A dose inicial recomendada de Ilaris é:
- Adultos e crianças de 2anos ou mais
- 150 mg para doentes que pesam mais de 40 kg
- 2 mg/kg para doentes que pesam entre 7,5 kg e menos de 40 kg
Ilaris é injectado cada 4 semanas como uma injeção única.
- Se não responder suficientemente ao tratamento aos 7 dias, o seu médico pode dar-lhe outra dose de 150 mg ou 2 mg/kg.
- Se responder suficientemente a esta, o seu tratamento continuará com 300 mg ou 4 mg/kg cada 4 semanas.
Doença de Still (AIJS e ESA)
A dose recomendada de Ilaris para doentes com doença de Still cujo peso corporal seja de 7,5 kg ou mais é de 4 mg/kg (até um máximo de 300 mg). Ilaris é injectado cada 4 semanas como uma dose única.
Gota artrítica
O seu médico discutirá consigo a necessidade de iniciar ou ajustar um tratamento com reductores de urato para diminuir o nível de ácido úrico do seu sangue.
A dose recomendada para Ilaris em doentes adultos com gota é 150 mg administrada como uma única dose durante um ataque de gota artrítica.
Se precisar de outro tratamento com Ilaris, e com a última dose obteve alívio, deve esperar um mínimo de 12 semanas antes de uma seguinte dose.
Autoinjeção de Ilaris ou injeção de Ilaris a um doente
Se é um doente com CAPS, TRAPS, HIDS/MKD, FMF ou doença de Still (ESA ou AIJS), ou um cuidador de um doente com uma destas doenças, pode administrar a si mesmo as injeções de Ilaris após receber uma formação adequada em relação à técnica de injeção.
- O doente ou cuidador e o médico decidirão quem vai injectar as injeções de Ilaris.
- O seu médico ou enfermeiro ensinar-lhe-á como injectar as injeções de Ilaris.
- Não deve tentar injectar-se se não recebeu a formação necessária ou não está seguro de como fazê-lo.
- Ilaris 150 mg pó para solução injectável é fornecido em um frasco de uso único para uso individual.
- Não reutilize a solução sobrante.
Para ter mais informações sobre como injectar as injeções de Ilaris, consulte a secção «Instruções de uso» no final deste prospecto. Se tiver dúvidas, fale com o seu médico, farmacêutico ou enfermeiro.
Duração do tratamento com Ilaris
- CAPS, TRAPS, HIDS/MKD, FMF ou doença de Still (ESA ou AIJS):deve continuar a usar Ilaris durante o tempo que o seu médico aconselhar.
- Gota artrítica:se tem um ataque de gota artrítica, será administrada uma única dose de Ilaris. Se experimentar um novo ataque, o seu médico pode considerar administrar-lhe uma nova dose de Ilaris, mas não antes de 12 semanas após a dose anterior.
Se usar mais Ilaris do que deve
Se injectar acidentalmente mais Ilaris do que a dose recomendada, não é provável que seja grave, mas deve informar o seu médico, farmacêutico ou enfermeiro o mais rápido possível.
Se esquecer de usar Ilaris
Se tem CAPS, TRAPS, HIDS/MKD ou FMF ou doença de Still (ESA ou AIJS) e esqueceu de se injectar uma dose de Ilaris, a dose seguinte deve ser injectada assim que possível. Então, fale com o médico para acordar quando deve injectar a dose seguinte. A seguir, deve seguir-se com a injeção aos intervalos recomendados como antes.
Se interromper o tratamento com Ilaris
A interrupção do seu tratamento com Ilaris pode causar um agravamento da sua doença. Não interrompa o tratamento com Ilaris a não ser que o seu médico o indique.
Se tiver alguma outra dúvida sobre o uso deste medicamento, pergunte ao seu médico, farmacêutico ou enfermeiro.
4. Efeitos adversos possíveis
Tal como todos os medicamentos, este medicamento pode produzir efeitos adversos, embora nem todas as pessoas os sofram.
Alguns efeitos adversos podem ser graves. Informe o seu médico imediatamente, se experimentar algum dos seguintes efeitos adversos:
- Febre que se prolongue por mais de 3 dias ou qualquer sintoma que possa sugerir uma infecção grave. Isso inclui tremores, calafrios, mal-estar geral, perda de apetite, dores no corpo, por lo geral relacionadas com a aparição súbita da doença, dor de garganta ou úlceras na boca, tosse, fleuma, dor no peito, dificuldade para respirar, dor de ouvido, dor de cabeça prolongada e enrubescimento, calor e inchação localizados na pele ou inflamação do tecido conjuntivo (celulite). Estes sintomas podem dever-se a uma infecção grave, uma infecção incomum (infecção oportunistica) ou estar relacionados com níveis baixos de glóbulos brancos (denominado leucopenia e neutropenia). Se o considerar necessário, o seu médico pode fazer-lhe análises de sangue de forma regular.
- Reações alérgicas com erupções cutâneas e prurido e possivelmente também urticária, dificuldade para respirar ou engolir, tontura, consciência incomum do batimento cardíaco (palpitações) e tensão arterial baixa.
Outros efeitos adversos de Ilaris incluem:
Muito frequentes(podem afetar mais de 1 em cada 10 pessoas):
- Infecções de qualquer tipo. Estas podem incluir:
- Infecções respiratórias, tais como infecção no peito, gripe, inflamação de garganta, secreção nasal, nariz entupido, espirros, sensação de pressão ou dor nas faces ou na testa com ou sem febre (pneumonia, bronquite, sintomas gripais, sinusite, rinite, faringite, tonsilite (dor de garganta), nasofaringite, infecção das vias respiratórias superiores).
- Outras infecções, como infecção de ouvido, infecção de pele (celulite), dor de estômago e gastroenterite e dor e necessidade de urinar frequentemente com ou sem febre (infecção do trato urinário).
- Dor abdominal superior.
- Dor nas articulações (artralgia).
- Descida nos níveis de glóbulos brancos (leucopenia).
- Resultados anormais da função renal (diminuição do clearance renal, proteinúria).
- Reações no local de injeção (tais como enrubescimento, inchação, calor e prurido).
Frequentes(podem afetar até 1 em cada 10 pessoas):
- Candida – infecção vaginal por fungos (candidíase vulvovaginal).
- Sentir-se tonto, sensação de que tudo gira (tontura ou vertigem).
- Dor nas costas ou músculos.
- Sensação de fraqueza ou muito cansado (fadiga, astenia).
- Descida nos níveis de glóbulos brancos que ajudam a prevenir a infecção (neutropenia).
- Níveis anormais de triglicérides no sangue (distúrbio do metabolismo lipídico).
- Resultados anormais do teste da função hepática (transaminases aumentadas) ou nível elevado de bilirrubina no sangue, com ou sem amarelamento da pele e olhos (hiperbilirrubinemia).
Pouco frequentes(podem afetar até 1 em cada 100 pessoas):
- Ardor (doença de refluxo gastroesofágico).
- Descida nos níveis das células sanguíneas que ajudam a prevenir as hemorragias (plaquetas).
Informar imediatamente o seu médico ou o médico do seu filho se notar algum destes sintomas.
Comunicação de efeitos adversos
Se experimentar qualquer tipo de efeito adverso, consulte o seu médico, farmacêutico ou enfermeiro, mesmo que se trate de possíveis efeitos adversos que não aparecem neste prospecto. Também pode comunicá-los diretamente através do sistema nacional de notificação incluído no Apêndice V. Mediante a comunicação de efeitos adversos, você pode contribuir para proporcionar mais informações sobre a segurança deste medicamento.
5. Conservação de Ilaris
- Manter este medicamento fora da vista e do alcance das crianças.
- Não utilize este medicamento após a data de validade que aparece na etiqueta e na caixa após CAD. A data de validade é o último dia do mês que se indica.
- Conservar na geladeira (entre 2 °C e 8 °C). Não congelar.
- Conservar no embalagem original para protegê-lo da luz.
- Depois de misturar o medicamento (reconstituição), deve ser utilizado imediatamente. Se não for utilizado imediatamente, deve ser conservado a solução na geladeira (2°C e 8°C) e utilizado nas seguintes 24 horas.
- Não utilize este medicamento se observar que a solução não é transparente a opalescente ou contém partículas.
- Todo medicamento não utilizado deve ser descartado após a injeção da dose.
Os medicamentos não devem ser jogados nos esgotos nem na lixeira. Pergunte ao seu farmacêutico como se livrar dos recipientes e dos medicamentos que já não precisa. Dessa forma, ajudará a proteger o meio ambiente.
6. Conteúdo do frasco e informações adicionais
Composição de Ilaris
- O princípio ativo é canakinumab. Cada frasco de pó contiene 150 mg de canakinumab. Após a reconstituição, cada ml de solução contém 150 mg de canakinumab.
- Os outros componentes são: sacarose, hidrocloruro de histidina monohidratado, polissorbato 80 (ver seção 2).
Aspecto do produto e conteúdo do frasco
- Ilaris é apresentado sob a forma de pó para solução injetável (150 mg em um frasco de vidro de 6 ml).
- O pó é branco.
- Ilaris está disponível em embalagens que contêm um frasco ou em caixas multiembalagem contendo 4 caixas intermediárias, cada uma das quais contém um frasco. Pode ser que apenas alguns tamanhos de embalagens sejam comercializados.
Título da autorização de comercialização
Novartis Europharm Limited
Edifício Vista
Elm Park, Merrion Road
Dublín 4
Irlanda
Responsável pela fabricação
Novartis Pharma GmbH
Roonstrasse 25
D-90429 Nürnberg
Alemanha
Novartis Pharma GmbH
Sophie-Germain-Strasse 10
90443 Nürnberg
Alemanha
Pode solicitar mais informações sobre este medicamento dirigindo-se ao representante local do titular da autorização de comercialização:
Bélgica Novartis Pharma N.V. Tel: +32 2 246 16 11 | Lituânia SIA Novartis Baltics Lietuvos filialas Tel: +370 5 269 16 50 |
Bulgária Novartis Bulgaria EOOD. Tel: +359 2 489 98 28 | Luxemburgo Novartis Pharma N.V. Tel: +32 2 246 16 11 |
República Tcheca Novartis s.r.o. Tel: +420 225 775 111 | Hungria Novartis Hungária Kft. Tel: +36 1 457 65 00 |
Dinamarca Novartis Healthcare A/S Tel: +45 39 16 84 00 | Malta Novartis Pharma Services Inc. Tel: +356 2122 2872 |
Alemanha Novartis Pharma GmbH Tel: +49 911 273 0 | Países Baixos Novartis Pharma B.V. Tel: +31 88 04 52 111 |
Estônia SIA Novartis Baltics Eesti filiaal. Tel: +372 66 30 810 | Noruega Novartis Norge AS Tel: +47 23 05 20 00 |
Grécia Novartis (Hellas) A.E.B.E. Tel: +30 210 281 17 12 | Áustria Novartis Pharma GmbH Tel: +43 1 86 6570 |
Espanha Novartis Farmacéutica, S.A. Tel: +34 93 306 42 00 | Polônia Novartis Poland Sp. z o.o. Tel: +48 22 375 4888 |
França Novartis Pharma S.A.S. Tel: +33 1 55 47 66 00 | Portugal Novartis Farma - Produtos Farmacêuticos, S.A. Tel: +351 21 000 8600 |
Croácia Novartis Hrvatska d.o.o. Tel: +385 1 6274 220 | Romênia Novartis Pharma Services Romania SRL Tel: +40 21 31299 01 |
Irlanda Novartis Ireland Limited Tel: +353 1 260 12 55 | Eslovênia Novartis Pharma Services Inc. Tel: +386 1 300 75 50 |
Islândia Vistor hf. Tel: +354 535 7000 | Eslováquia Novartis Slovakia s.r.o. Tel: +421 2 5542 5439 |
Itália Novartis Farma S.p.A. Tel: +39 02 96 54 1 | Finlândia Novartis Finland Oy Tel: +358 (0)10 6133 200 |
Chipre Novartis Pharma Services Inc. Tel: +357 22 690 690 | Suécia Novartis Sverige AB Tel: +46 8 732 32 00 |
Letônia SIA Novartis Baltics. Tel: +371 67 887 070 |
Data da última revisão deste prospecto:
Outras fontes de informação
A informação detalhada sobre este medicamento está disponível no site da Agência Europeia de Medicamentos: https://www.ema.europa.eu
Instruções de uso de Ilaris pó para solução injetável
Por favor, note que a preparação da injeção pode levar cerca de 30 minutos.
Consulte também a seção 3, «Autoinjeção de Ilaris ou injeção de Ilaris em um paciente».
Leia estas instruções por completo antes de começar.
Preparativos essenciais:
- Encontre um local limpo para preparar e administrar a injeção.
- Lave as mãos com água e sabão.
- Verifique a data de validade do frasco e da seringa. Não os use após a data de validade que aparece na etiqueta e na embalagem. A data de validade é o último dia do mês indicado.
- Use sempre seringas e agulhas novas que estejam em embalagens fechadas. Evite o contato com as agulhas e o plugue do frasco.
Reúna todos os elementos necessários:
Incluídos na embalagem
- um frasco de Ilaris pó para solução injetável (manter na geladeira).
Não incluídos na embalagem
- um frasco (ou ampola) de água estéril para injeção («água») (à temperatura ambiente)
- uma seringa de 1,0 ml
- uma agulha de 18 G x 2 polegadas (50 mm) para reconstituir o pó («agulha para transferência»)
- uma agulha de 27 G x 0,5 polegadas (13 mm) para a injeção («agulha de injeção»)
- comprimidos de algodão
- algodão seco e limpo
- um adesivo
- um recipiente apropriado para depositar as agulhas, seringa e o frasco usados (recipiente de material de descarte)
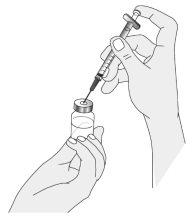
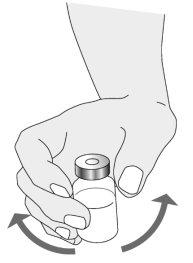
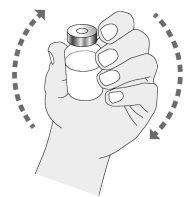
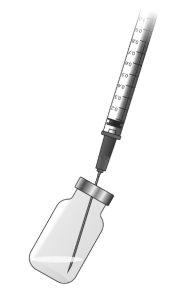
Preparação da mistura de Ilaris
|
|
|
|
|
|
|
|
|
|
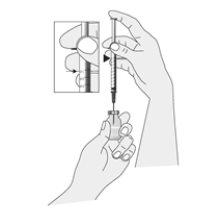
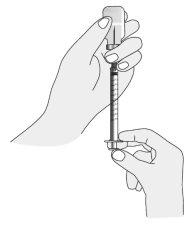
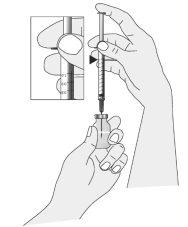
Preparação da injeção
|
|
|
|
|
|
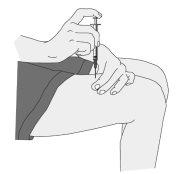
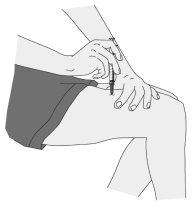
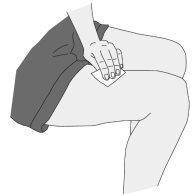
Administração da injeção
|
|
|
|
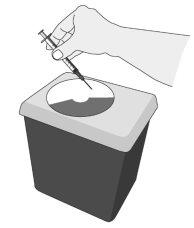
Após a injeção
|
|
|
Mantenha o recipiente de material de descarte fora da vista e do alcance das crianças. Elimine-o de acordo com as instruções recebidas do profissional de saúde ou farmacêutico. |
- País de registo
- Forma farmacêuticaINJETÁVEL, 150 mg/ml de canakinumabe
- Código ATCL04AC08
- Substância ativa
- Requer receita médicaSim
- Fabricante
- Esta informação é apenas para fins informativos e não constitui aconselhamento médico. Consulte sempre um médico antes de tomar qualquer medicamento.
- Alternativas a ILARIS 150 mg PÓ PARA SOLUÇÃO INJETÁVELForma farmacêutica: INJETÁVEL, 150 mg/mlSubstância ativa: canakinumabFabricante: Novartis Europharm LimitedRequer receita médicaForma farmacêutica: PERFURAÇÃO INJETÁVEL, 130 mgSubstância ativa: ustekinumabFabricante: Accord Healthcare S.L.U.Requer receita médicaForma farmacêutica: INJETÁVEL, 45 mgSubstância ativa: ustekinumabFabricante: Accord Healthcare S.L.U.Requer receita médica
Médicos online para ILARIS 150 mg PÓ PARA SOLUÇÃO INJETÁVEL
Avaliação de dosagem, efeitos secundários, interações, contraindicações e renovação de receita para ILARIS 150 mg PÓ PARA SOLUÇÃO INJETÁVEL — sujeita a avaliação médica e à regulamentação local.
Obtenha uma receita de ILARIS 150 mg PÓ PARA SOLUÇÃO INJETÁVEL online
Preencha um formulário de 2 minutos
Conte-nos os seus sintomas, historial e o medicamento que está a solicitar.
Escolha um médico ou deixe-nos atribuir
Escolha um especialista ou ligamos com o próximo médico disponível.
O médico analisa o seu caso
Normalmente em 30 minutos. Pode fazer perguntas adicionais por chat.
Levante em qualquer farmácia
Receita eletrónica enviada para o seu e-mail — válida em toda a Espanha.
Perguntas frequentes

Receba atualizações e ofertas exclusivas
Seja o primeiro a conhecer novos serviços, atualizações do marketplace e ofertas exclusivas para subscritores.